Parte III: |
La malnutrición proteinoenergética (MPE) en los niños pequeños es en la actualidad el problema nutricional más importante en casi todos los países en Asia, América Latina, el Cercano Oriente y África. La carencia de energía es la causa principal. No hay cifras mundiales exactas sobre la prevalencia de MPE, pero los cálculos de la Organización Mundial de la Salud (OMS) estiman que la frecuencia de MPE en niños menores de cinco años en los países en desarrollo ha disminuido progresivamente de 42,6 por ciento en 1975, a 34,6 por ciento en 1995. Sin embargo, en algunas regiones esta disminución relativa no ha sido tan rápida como el aumento de la población; por lo tanto en algunas regiones, como África y el sudeste de Asia, el número total de niños desnutridos ha aumentado. En realidad, el número de niños con peso bajo en el mundo entero aumentó de 195 millones en 1975 a casi 200 millones a finales de 1994, lo que significa que más de una tercera parte de la población mundial menor de cinco años de edad está desnutrida.
Una falla en el crecimiento es la primera y la más importante manifestación de MPE. A menudo es el resultado de consumir muy pocos alimentos ricos en energía, y no es raro que esto se agrave a cauda de infecciones. Un niño que tenga carencias en su crecimiento puede ser de menor estatura, o puede estar por debajo del peso de un niño de su edad, o puede ser más delgado de lo que corresponde a su altura.
El marco conceptual descrito en el Capítulo 1 sugiere que hay tres condiciones necesarias para evitar la malnutrición o los problemas de crecimiento: disponibilidad y consumo de alimentos adecuados; buena salud y acceso a servicios médicos; y una atención y prácticas alimentarias adecuadas. Si falta una de ellas, el probable resultado es la MPE.
El término malnutrición proteinoenergética se incorporó a la literatura médica hace poco tiempo, pero el problema se conocía desde muchos años atrás. En las primeras publicaciones se le llamó con otros nombres, como desnutrición proteico-energética y deficiencia proteico-energética.
El término MPE se emplea para describir una gama amplia de condiciones clínicas que van desde moderadas a graves. En un extremo del espectro, la MPE moderada se manifiesta principalmente por retardo en el crecimiento físico de los niños; y en el extremo opuesto, el kwashiorkor (caracterizado por la presencia de edema) y el marasmo nutricional (que se distingue por una aguda emaciación); en ambos casos se registran altas tasas de mortalidad.
Durante siglos se ha sabido que la ingesta pobre durante hambrunas y la escasez grave de comida llevan a la pérdida de peso y al agotamiento, y, eventualmente a la muerte por inanición. En la década de 1930 Cicely Williams, que trabajaba en Ghana, describió en detalle la condición que denominó «kwashiorkor» (utilizó la palabra ghanesa local que significa «la enfermedad del niño desplazado»). En la década de 1950, el kwashiorkor empezó a recibir más atención. Con frecuencia se describió como la forma más importante de malnutrición y se consideró que se debía sobre todo a carencia de proteína. Parecía que la solución era producir más alimentos ricos en proteína y ponerlos a disposición de los niños en riesgo. Este énfasis en el kwashiorkor y en la proteína llevó a una relativa falta de atención para el marasmo nutricional y sobre el consumo adecuado de alimentos ricos en energía para los niños.
El punto de vista actual consiste en que buena parte de la MPE se debe a un consumo inadecuado o a la mala utilización de alimentos y energía, no a carencia de un solo nutriente, ni tampoco a la falta de proteína alimentaria. También se acepta cada vez más que las infecciones contribuyen en forma importante a la MPE. Se sabe ahora que el marasmo nutricional predomina más que el kwashiorkor. No se sabe por qué un niño puede desarrollar un síndrome en oposición a otro, y ahora se acepta que estas dos formas clínicas de MPE constituyen apenas una punta pequeña del iceberg. En casi todas las poblaciones estudiadas en países pobres, la tasa de prevalencia combinada de kwashiorkor y marasmo nutricional es de 1 a 5 por ciento, mientras que del 30 al 70 por ciento de los niños hasta los cinco años manifiestan lo que ahora se llama MPE leve o moderada, que se diagnostica principalmente con base en mediciones antropométricas.
CAUSAS Y EPIDEMIOLOGÍA
La MPE - no como otras enfermedades nutricionales importantes por carencia - se debe a una falta de macronutrientes, no a escasez de micronutrientes. Aunque se denomina MPE, se acepta ahora, por lo general, que se debe en muchos casos a una carencia de energía, casi siempre producida por consumo insuficiente de alimentos. Esta carencia de energía es más importante y más común que la carencia de proteína. No es raro que se asocie con infecciones y con falta de micronutrientes. El cuidado incorrecto, por ejemplo comidas poco frecuentes, puede desempeñar un papel importante.
Sin embargo, la causa de la MPE (y de otras enfermedades por carencia que predominan en los países en desarrollo) no se debe considerar tan sólo en términos de consumo escaso de nutrientes. Para una nutrición satisfactoria, los alimentos y los nutrientes que contienen deben estar disponibles para la familia en cantidad adecuada; se ha de suministrar una cantidad correcta y equilibrada de alimentos y nutrientes a intervalos regulares; el individuo debe tener deseos de consumir los alimentos; y tener una digestión y una absorción apropiadas de nutrientes y alimentos; el metabolismo de la persona debe ser razonablemente normal; y no tener trastornos que impidan que las células corporales utilicen los nutrientes o que se produzcan pérdidas anormales de ellos. Los factores que influyen de modo negativo sobre cualquiera de estos requisitos pueden ser causas de malnutrición, en particular la MPE. La etiología, por lo tanto, puede ser compleja. Ciertos factores que contribuyen a la MPE especialmente en el niño pequeño, se relacionan con el huésped, el agente (la dieta) y el medio. Las causas subyacentes también se pueden clasificar dentro de las relacionadas con la seguridad alimentaria del niño, salud (incluso prevención de infecciones y tratamiento adecuado de las enfermedades) y cuidado, que incluyen las prácticas maternas y familiares, como las que tienen que ver con la frecuencia de la alimentación, lactancia y destete.
Algunos ejemplos de factores comprometidos en la etiología de la MPE son:
las necesidades elevadas de energía y proteína por kilogramo de peso del niño, respecto a las de los miembros mayores de la familia;
prácticas incorrectas de destete;
uso inapropiado de la fórmula láctea infantil en vez de la lactancia natural para el niño en las familias pobres;
dietas básicas que a menudo son de baja densidad energética (con frecuencia en cantidades grandes pero poco apetitosas), bajas en contenido de proteína y grasa, y que no se dan a los niños con la regularidad necesaria;
poco cuidado de los niños debido, por ejemplo, a restricciones de tiempo para la madre o a ignorancia sobre la calidad y el valor de la lactancia exclusiva;
disponibilidad poco adecuada de alimentos para la familia debido a pobreza, desigualdad económica o falta de suficiente terreno cultivable, y problemas que se relacionan con la distribución de los alimentos dentro de la familia;
infecciones (virales, bacterianas y parasitarias) que pueden causar anorexia, reducir el consumo de alimentos, evitar la absorción y el aprovechamiento de nutrientes o que originan pérdida de éstos; hambruna resultante de sequías, desastres naturales, guerras, desórdenes civiles, etc. (Foto 15).
La prematurez o el bajo peso al nacer puede predisponer al niño a desarrollar el marasmo nutricional. En las sociedades pobres también lo pueden causar el fracaso de la lactancia debido a la separación o a la muerte de la madre, o la falta o insuficiencia de leche materna, pues la lactancia casi siempre es la única forma factible en que las madres alimentan a sus bebés en forma adecuada. Una causa subyacente de MPE es todo factor que impide que las madres amamanten a sus niños recién nacidos, cuando viven en hogares donde puede ser difícil o peligrosa la alimentación con biberón. Por lo tanto, la promoción de fórmulas lácteas infantiles así como el apoyo insuficiente a la lactancia natural por parte de los médicos o de los servicios de salud, pueden ser factores en la epidemiología del marasmo. La lactancia exclusiva prolongada, sin que se den otros alimentos después de los seis meses de edad, puede también contribuir a la falta de crecimiento, a la MPE y eventualmente, al marasmo nutricional.
Creer que el kwashiorkor resulta de una carencia de proteína, y que el marasmo nutricional se debe a falta de energía en los alimentos, es una excesiva simplificación, porque las causas de ambas entidades son complejas. En efecto, hay factores tanto endógenos como exógenos que pueden determinar si un niño desarrolla marasmo nutricional, kwashiorkor o la forma intermedia conocida como kwashiorkor marásmico. En un niño que consume mucho menos alimento del necesario para suplir a sus necesidades de energía, ésta se obtiene a partir de la grasa corporal y del músculo. Aumenta la gluconeogénesis en el hígado y, hay pérdida de grasa subcutánea y agotamiento muscular. Se ha sugerido que en estas circunstancias, sobre todo cuando el consumo de proteína es muy bajo con respecto al consumo de carbohidratos (y si la situación se agrava quizá por pérdidas de nitrógeno a causa de infecciones), se llevan a cabo diversos cambios metabólicos que pueden contribuir al desarrollo del edema. Se retienen más sodio y agua, y gran parte de ésta se acumula fuera del sistema cardiovascular, en los tejidos, y se produce un edema oculto. El papel verdadero de la infección no se ha explicado de modo satisfactorio, pero ciertas infecciones producen mayor aumento del nitrógeno urinario, que viene de los aminoácidos del tejido muscular.
No hay consenso sobre la causa verdadera del edema que es característico del kwashiorkor. Casi todos los investigadores están de acuerdo en que la carencia de potasio y la retención de sodio son importantes en la patogénesis del edema. Hay pruebas en favor del argumento clásico que la malnutrición edematosa es un signo de consumo inadecuado de proteína. Por ejemplo, el edema, el hígado graso y una condición semejante al kwashiorkor se pueden inducir en cerdos y mandriles con una dieta baja en proteína. La evidencia epidemiológica además muestra mayores tasas de kwashiorkor en Uganda - donde la dieta básica es el plátano, que tiene un contenido muy bajo de proteína - con respecto a las áreas vecinas donde el alimento básico es un cereal.
Recientemente se han propuesto dos teorías nuevas para explicar la causa del kwashiorkor. La primera afirma que el kwashiorkor se debe a envenenamiento por aflatoxina. La segunda sostiene que los radicales libres son importantes en la patogénesis del síndrome, dado que la mayoría de las características clínicas del kwashiorkor se podrían originar en un exceso de radicales libres. Esta teoría novedosa, aún por demostrar, también sugiere que el kwashiorkor, aunque producido por radicales libres, quizá atacaría tan sólo a niños con carencia de consumo de alimentos y que estén expuestos a infecciones. Por lo tanto, si se comprueba que esta teoría es correcta, apenas explicaría un mecanismo en la patogénesis del kwashiorkor. No cambia el hecho que si se mejora la dieta y si se controlan las infecciones se logra una reducción importante del kwashiorkor y del marasmo nutricional. Ni la teoría de la aflatoxina ni la de los radicales libres se han demostrado de modo experimental, tampoco hay estudios adecuados decisivos para sustentar la hipótesis de la falta de adaptación individual como causa de un MPE grave. Sorprende que ninguna investigación haya podido probar de modo definitivo ya sea la semejanza o la diferencia en el consumo alimentario de los niños que desarrollan kwashiorkor con edema y los que muestran signos clínicos de marasmo nutricional sin edema.
Por lo general en los casos de MPE grave hay indicios clínicos y muchas veces comprobación bioquímica de carencias de micronutrientes, lo que no sorprende si el niño o el adulto consumen una dieta inadecuada. Tanto en el marasmo nutricional como en el kwashiorkor (y además en la MPE moderada), los exámenes clínicos o las pruebas bioquímicas, a menudo registran, por ejemplo, carencia de vitamina A, anemia nutricional y/o carencia de zinc. Sin embargo, no está comprobado que alguna carencia de micronutrientes sea la causa principal de la MPE o que por sí misma sea responsable del edema en el kwashiorkor.
Sin tener en cuenta qué teoría o etiología demuestre ser la correcta, es posible prevenir la MPE si se mejora la cantidad de alimentos consumidos, si se dan los pasos adecuados para garantizar que las dietas sean nutricionalmente bien equilibradas y si se controlan las infecciones.
MANIFESTACIONES Y CUADRO CLÍNICO
MPE
leve y moderada
La condición de la MPE a menudo se compara con un iceberg, donde un 20 por ciento es visible por encima del agua y casi el 80 por ciento se encuentra sumergido. Las formas graves de MPE - kwashiorkor, marasmo nutricional y kwashiorkor marásmico - son la parte superior expuesta del iceberg, relativamente fáciles de identificar por un médico o un trabajador de salud, tan sólo por sus manifestaciones clínicas, que se describen a continuación. Por otra parte, los niños con malnutrición moderada o leve a menudo no tienen manifestaciones clínicas claras de desnutrición; son de menor estatura y/o más delgados de lo que se esperaría para su edad, y pueden tener déficit en el desarrollo psicológico y quizás otros signos no tan fáciles de demostrar. La MPE leve y moderada se diagnostica principalmente basada en la antropometría, en especial usando mediciones de peso y altura y algunas veces con otras mediciones, como la circunferencia del brazo o el espesor de los pliegues cutáneos.
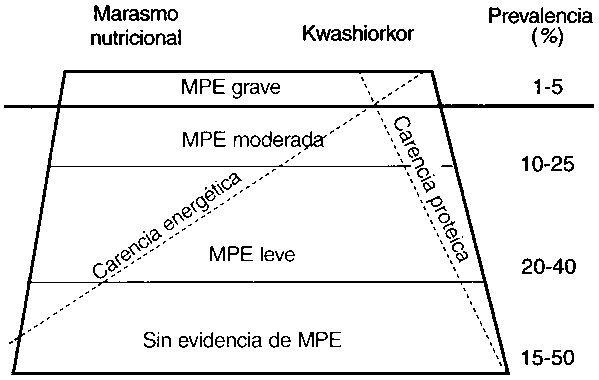
Como se indicó en el diagrama del iceberg (Figura 5), la prevalencia de MPE más visible y seria (kwashiorkor, kwashiorkor marásmico y marasmo nutricional) por lo general está entre el 1 y el 5 por ciento, excepto en áreas de hambruna. Por el contrario, la malnutrición moderada y leve alcanza del 30 al 70 por ciento en muchos países de África subsahariana y del sudeste asiático. En estas áreas, sólo de 15 a 30 por ciento de los niños entre seis y 60 meses de edad no muestran evidencias de MPE. El diagrama ilustra que los déficit de energía y de proteína son parte del problema, pero que la carencia de energía es la más importante. Sugiere también que la falta de proteína juega un papel muy importante en el kwashiorkor y la carencia energética en el marasmo nutricional.
El porcentaje de niños clasificados con MPE grave, moderada y leve depende de cómo se definen estos términos. Las dos formas graves de malnutrición, kwashiorkor y marasmo nutricional, tienen aspectos y características clínicas muy diferentes, como se verá a continuación. Por lo general, se acepta que la característica del kwashiorkor es el edema en moneda, y que la del marasmo nutricional es el bajo peso. A los niños que tienen edema y un serio bajo peso se les diagnostica kwashiorkor marásmico.
FIGURA 5 Iceberg de la MPE
La clasificación de MPE denominada Wellcome se ha utilizado ampliamente por más de 20 años (véase el Cuadro 19). Tiene la ventaja de la simplicidad, pues se basa sólo en dos indicadores, el porcentaje de peso estándar para la edad y la presencia o ausencia de edema. La categoría «desnutrido» incluye niños que tienen MPE moderada o moderadamente grave pero sin edema y cuyo peso está por encima del 60 por ciento del estándar. Hoy, se considera más apropiado un punto de corte con desviaciones estándar (DE) que el porcentaje de peso estándar para la edad, pero no se podría volver a reclasificar a muchos niños.
En las décadas de 1950 y 1960 el grado de malnutrición casi siempre se basó en el porcentaje de peso estándar para la edad del niño. En América Latina y en otras partes, se usó ampliamente la clasificación de Gómez (Cuadro 20).
CUADRO 19
Clasificación Wellcome: formas graves de malnutrición proteinoenergética
|
Porcentaje de peso estándar para la edad |
Presencia de edema |
Ausencia de edema |
|
60-80 |
Kwashiorkor |
Desnutrición |
|
<60 |
Kwashiorkor marásmico |
Marasmo nutricional |
CUADRO 20
Clasificación de Gómez: malnutrición basada en peso
estándar para la edad
|
Clasificación |
Porcentaje de peso estándar para la edad |
|
Normal |
>90 |
|
Grado I |
75-89,9 |
|
Grado II |
60-74,9 |
|
Grado IIIa |
<60 |
a J. Bengoa de la OMS sugirió que todos los niños con edema se deberían clasificar en grado III. Esto se conoce como la modificación Bengoa.
A principios de la década de 1970, un grupo de trabajadores de la salud empezó a sugerir que juzgar el grado de malnutrición sólo basado en el peso por edad tenía muchas desventajas. Se propuso un método que distinguía tres categorías de MPE (leve a moderada), basado en el peso y altura de los niños. Posteriormente estas categorías se conocieron como:
Emaciación: manifestación aguda de malnutrición de corta duración, donde el peso para la edad y la estatura son bajos, pero la altura para la edad es normal;
Detención del crecimiento: malnutrición crónica previa donde el peso y la estatura para la edad son bajos, pero el peso para la altura es normal;
Emaciación y detención del crecimiento: malnutrición aguda y crónica o malnutrición actual de larga duración, donde el peso, la estatura para la edad y el peso para la altura son todos bajos.
Esta clasificación establece una distinción entre los factores actuales y pasados en el estado nutricional. Ayuda al examinador a evaluar la probabilidad de que la alimentación suplementaria mejore notoriamente el estado nutricional del niño, y le brinde al médico clínico algunas pautas clave en cuanto a la historia de malnutrición del enfermo. Además tiene ventajas para las encuestas de nutrición y de seguimiento nutricional. Generalmente, la detención del crecimiento predomina más que la emaciación en el mundo entero.
Como se discute en el Capítulo 33, que trata sobre la evaluación del estado nutricional, hoy se recomienda clasificar la malnutrición basada en desviaciones estándar, por debajo de las normas de crecimiento del Centro Nacional para Estadísticas de Salud de los Estados Unidos (NCHS) publicadas por la OMS. En los informes por país basados sólo en peso para la edad, el término «poco peso» se emplea por lo general para indicar un peso por debajo de 2 DE de las normas NCHS para niños hasta cinco años de edad. En una distribución normal se espera que de 2 a 3 por ciento de los niños estén por debajo del punto de corte de -2 DE. Una prevalencia por encima de ese nivel sugiere un problema nutricional en la población en estudio. Si además se toman las mediciones considerando a la estatura, entonces se pueden dividir los niños en los que tienen emaciación, detención del crecimiento o ambos síndromes.
Los responsables de las políticas y los trabajadores de salud necesitan decidir qué tipo de patrones de crecimiento van a utilizar como norma para juzgar la malnutrición y para las encuestas, seguimiento y vigilancia en este campo. En los últimos años las normas de crecimiento OMS/NCHS (que no difieren mucho de las normas utilizadas anteriormente, como las normas de Harvard y de Denver sobre crecimiento) han tenido mayor aceptación. Se ha visto que las normas internacionales de crecimiento son aplicables a los países en desarrollo, como lo muestra la evidencia que el crecimiento en los niños de clases pudientes en los países en desarrollo no difiere en forma importante de tales normas, y que el menor crecimiento que se observa en los menos favorecidos es resultado de factores sociales, donde se incluye el complejo malnutrición-infección, y no diferencias étnicas o geográficas.
La importancia funcional de la MPE leve o moderada, todavía no se conoce bien. Los estudios en varios países indican que el riesgo de mortalidad aumenta con rapidez cuando empeora el estado nutricional de acuerdo con los indicadores antropométricos. Investigaciones recientes en Guatemala indican que los adolescentes con crecimiento insuficiente cuando se examinaron en la primera infancia, eran más pequeños en estatura, les iba menos bien en el colegio, su estado físico era más pobre y sus puntajes eran más bajos en las pruebas de desarrollo psicológico que los niños de las mismas ciudades que tuvieron mejor crecimiento durante la infancia. Estos resultados sugieren las consecuencias a largo plazo de la MPE en los primeros años de vida.
El propósito de controlar la extensión y gravedad de la MPE mediante gran número de estrategias y distintas acciones es un punto crítico en las políticas y programas nutricionales para la mayoría de los países en desarrollo. La reducción y prevención eventual de la malnutrición leve y moderada, automáticamente reducirá la malnutrición grave. Por lo tanto, aunque puede ser tentador (sobre todo para los médicos y otros trabajadores de la salud) dar un énfasis mayor al control del marasmo nutricional y del kwashiorkor, los recursos a menudo se emplean mejor controlando la MPE leve y moderada, lo que a su vez reducirá la MPE grave.
KWASHIORKOR
El kwashiorkor es una de las formas serias de la MPE. Se observa a menudo en niños de uno a tres años de edad, pero puede aparecer a cualquier edad. Se encuentra en niños que tienen una dieta por lo general baja en energía y proteína y también en otros nutrientes. A menudo los alimentos suministrados al niño son principalmente carbohidratos; alimentos de mucho volumen que además no se suministran frecuentemente.
El kwashiorkor es común que se asocie con enfermedades infecciosas, que, inclusive, lo pueden precipitar. La diarrea, infecciones respiratorias, sarampión, los ferina, parásitos intestinales y otras entidades clínicas son causas habituales subyacentes de MPE y pueden hacer que los niños desarrollen el kwashiorkor o el marasmo nutricional. Estas infecciones por lo general producen pérdida del apetito, que es una causa importante de la MPE grave. Las infecciones, especialmente las que se acompañan de fiebre, ocasionan una mayor pérdida de nitrógeno en el organismo, que sólo se puede reemplazar con una dieta con proteínas.
Signos clínicos del kwashiorkor
El kwashiorkor es relativamente fácil de diagnosticar teniendo en cuenta la historia clínica del niño, los síntomas y los signos observados (Figura 6). Las pruebas de laboratorio no son esenciales pero dan algo de luz. Todos los casos de kwashiorkor presentan edema hasta cierto grado, fallas en el crecimiento, disminución de los músculos e infiltración grasa del hígado. Otros signos incluyen cambios mentales, anormalidades en el cabello, dermatosis típica, anemia, y diarrea, así como carencias de otros micronutrientes (Fotos 16 y 17).
Edema. La acumulación de líquido en los tejidos hace que se hinchen; en el kwashiorkor esta condición se encuentra presente casi siempre hasta cierto grado. De modo usual empieza con una ligera hinchazón de los pies y no es raro que se extienda a las piernas. Más adelante, también se hinchan las manos y la cara. Para diagnosticar la presencia de edema el encargado de la atención de salud presiona con un dedo o el pulgar sobre el tobillo. Si hay presencia de edema, la depresión que se forma toma unos segundos para volver al nivel de la piel.
Crecimiento deficiente. Siempre hay una carencia en el crecimiento. Si se sabe la edad precisa del niño, se encontrará que es más pequeño de lo normal y, excepto en casos de edema evidente, tendrá menor peso de lo normal (casi siempre de 60 a 80 por ciento del estándar o por debajo de 2 DE). Estos signos se pueden enmascarar por el edema o si se ignora la edad del niño.
FIGURA 6
Características del kwashiorkor
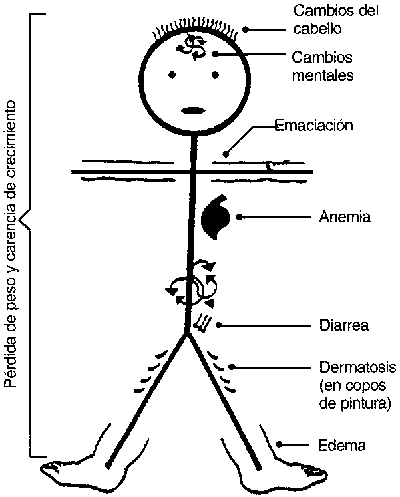
Emaciación. La emaciación también es típica, pero puede no descubrirse por el edema. Los brazos y piernas del niño son delgados debido a la pérdida de masa muscular.
Infiltración grasa del hígado. Siempre se halla en el examen postmortem de casos de kwashiorkor. Puede causar agrandamiento palpable del hígado (hepatomegalia).
Cambios mentales. Los cambios mentales son comunes pero no siempre se perciben. El niño por lo general es apático con su entorno e irritable cuando se le mueve o molesta. Prefiere permanecer en una misma posición y casi siempre está triste y no sonríe. Es raro que tenga apetito.
Cambios en el cabello. El cabello de los niños asiáticos, africanos o latinoamericanos normales es generalmente de color negro oscuro, de textura gruesa y con un brillo saludable que refleja la luz. En el kwashiorkor, el cabello se vuelve más sedoso y delgado. El cabello africano pierde su consistencia apretada. Al mismo tiempo carece de brillo, es opaco y sin vida y puede cambiar su color a castaño o castaño rojizo. Algunas veces se pueden arrancar con facilidad mechones pequeños y casi sin dolor. Al examen con microscopio, el cabello arrancado exhibe cambios en la raíz y un diámetro más estrecho que el cabello normal. La resistencia tensil del cabello también disminuye. En América Latina, se han descrito bandas de cabello descolorido como signo del kwashiorkor. Estas líneas de cabello castaño rojizo se han denominado «signo de bandera» o «signa bandera».
Cambios en la piel. La dermatosis aparece en algunos pero no en todos los casos de kwashiorkor. Tiende a aparecer primero en las áreas de fricción o de presión, como las ingles, detrás de las rodillas y en el codo. Aparecen parches pigmentados oscuros, que se pueden pelar o descamar con facilidad. La semejanza de estos parches con pintura seca, quemada por el sol, ha dado origen al término «dermatosis de pintura en copos». Por debajo de los copos de piel hay áreas atróficas no pigmentadas, que pueden parecer la cicatrización de una quemadura.
Anemia. Casi todos los casos tienen algún grado de anemia debido a la falta de la proteína que se necesita para producir células sanguíneas. La anemia se puede complicar por carencia de hierro, malaria, uncinariasis, etc.
Diarrea. Las heces por lo común son sueltas y con partículas de alimentos no digeridos. Algunas veces tienen olor desagradable o son semilíquidas o teñidas con sangre.
Cara de luna. Las mejillas pueden parecer hinchadas ya sea con tejido graso o líquido, y dar la apariencia característica que se conoce como «cara de luna».
Signos de otras carencias. En el kwashiorkor por lo general se puede palpar algo de grasa subcutánea y la cantidad ofrece una indicación del grado de carencia de energía. Los cambios en la boca y los labios, característicos de la falta de vitamina B son comunes. Se puede observar la xerosis o la xeroftalmía resultante de la falta de vitamina A. También se pueden presentar carencias de zinc y de otros micronutrientes.
Diagnóstico diferencial
Nefrosis. El edema es también una característica de la nefrosis, que se puede confundir con el kwashiorkor. En la nefrosis, sin embargo, la orina contiene mucha albúmina, así como cilindros y células. En el kwashiorkor, por lo general sólo hay trazas de albúmina. Si se encuentra dermatosis en copos de pintura u otros signos de kwashiorkor, se establece el diagnóstico. No es raro observar ascitis en la nefrosis, pero sólo rara vez en el kwashiorkor. En la mayoría de los países en desarrollo el kwashiorkor es una causa mucho más común de edema que la nefrosis.
Anemia grave por uncinariasis. El edema se puede deber sólo a esta causa. En los niños pequeños, el kwashiorkor también se encuentra e menudo presente. En la anemia causada por uncinarias no hay cambios en la piel distintos a la palidez. En todos los casos hay que examinar la materia fecal.
Disentería crónica. En esta enfermedad el edema no es una característica.
Pelagra. La pelagra es rara en niños pequeños. Las lesiones de la piel son algunas veces semejantes a las del kwashiorkor, pero en la pelagra tienden a presentarse en áreas expuestas a la luz solar (no en las ingles, por ejemplo). No es raro que se acompañe con diarrea y pérdida de peso, pero sin edema o cambios en el cabello.
MARASMO NUTRICIONAL
En la mayoría de los países el marasmo, la otra forma grave de MPE, predomina ahora mucho más que el kwashiorkor. En el marasmo, la principal carencia es de alimentos en general, y por lo tanto, también de energía. Puede suceder a cualquier edad, sobre todo hasta alrededor de tres años y medio, pero en contraste con el kwashiorkor, es más común durante el primer año de vida. El marasmo nutricional es en realidad una forma de hambre, y las posibles causas subyacentes son numerosas. Por cualquier razón, el niño no recibe cantidad suficiente de leche materna o de cualquier alimento alternativo.
CUADRO 21
Comparación de las características del kwashiorkor y el marasmo
|
Característica |
Kwashiorkor |
Marasmo |
|
Insuficiente crecimiento |
Presente |
Presente |
|
Emaciación |
Presente |
Presente, notorio |
|
Edema |
Presente (algunas veces leve) |
Ausente |
|
Cambios en el cabello |
Común |
Menos común |
|
Cambios mentales |
Muy común |
Raros |
|
Dermatosis, copos de pintura |
Común |
No ocurre |
|
Apetito |
Pobre |
Bueno |
|
Anemia |
Grave (algunas veces) |
Presente, menos grave |
|
Grasa subcutánea |
Reducida pero presente |
Ausente |
|
Rostro |
Puede ser edematoso |
Macilento, cara de mono |
|
Infiltración grasa del hígado |
Presente |
Ausente |
Quizás las causas precipitantes más importantes del marasmo son las infecciones y enfermedades parasitarias de la infancia. Estas incluyen sarampión, los ferina, diarrea, malaria, y otras debidas a parásitos. Las infecciones crónicas como la tuberculosis pueden también llevar al marasmo. Otras causas comunes del marasmo son el parto prematuro, la deficiencia mental y las molestias digestivas, como malabsorción o vómito. Una causa muy común es también la interrupción temprana de la lactancia.
Características clínicas del marasmo nutricional
Las características principales del kwashiorkor y el marasmo nutricional se comparan en el Cuadro 21. A continuación se describen los principales signos de marasmo (Fotos 18 y 19).
Crecimiento deficiente. En todos los casos el niño no crece en forma adecuada. Si se conoce la edad, el peso será muy bajo según los estándares normales (por debajo de 60 por ciento o -3 DE del estándar). En los casos graves la pérdida muscular es obvia: las costillas sobresalen; el estómago, en contraste con el resto del cuerpo, puede ser protuberante; la cara tiene una característica simiesca (como un mono); y las extremidades inferiores son muy delgadas. El niño parece ser sólo piel y huesos. Un caso avanzado de la enfermedad es inconfundible, y una vez que se ve, jamás se olvida.
Emaciación. Los músculos siempre se encuentran muy disminuidos. Hay poca grasa subcutánea, si es que queda algo. La piel cuelga en arrugas, sobre todo alrededor de las nalgas y los muslos. Cuando se toma la piel entre el índice y el pulgar se nota la ausencia de la capa habitual de tejido adiposo.
Estado de alerta. Los niños con marasmo raramente son desinteresados como los que sufren kwashiorkor. Los ojos profundamente hundidos les dan una apariencia bastante despierta. También se puede manifestar en modo menos infeliz e irritable.
Apetito. El niño por lo general tiene buen apetito. En realidad, como cualquier individuo hambriento, el niño puede ser voraz. Los niños con marasmo a menudo se chupan las manos violentamente o la ropa o cualquier otra cosa a su alcance. Algunas veces emiten sonidos de succión.
Anorexia. Algunos niños son anoréxicos.
Diarrea. La materia fecal puede ser suelta, pero no es una característica constante de la enfermedad. La diarrea de naturaleza infecciosa, como ya se mencionó, puede comúnmente haber sido un factor precipitante.
Anemia. Casi siempre se encuentra anemia.
Ulceraciones en la piel. Puede haber úlceras por presión, pero por lo general están sobre las prominencias óseas, no en áreas de fricción. En contraste con el kwashiorkor, no existe edema y en el marasmo no hay dermatosis en copos de pintura.
Cambios del cabello. Puede haber cambios semejantes a los del kwashiorkor. Es más común un cambio en la textura que en el color.
Deshidratación. Aunque por sí misma no es una característica de la enfermedad, es común que la deshidratación acompañe al marasmo; como resultado de una fuerte diarrea (y algunas veces del vómito).
KWASHIORKOR MARÁSMICO
A los niños con características de marasmo nutricional y kwashiorkor se les clasifica como kwashiorkor marásmico. Según la clasificación de Wellcome (véase más arriba) se da este diagnóstico a todo niño con malnutrición grave que tiene edema y un peso por debajo de 60 por ciento de lo esperado para la edad. Los niños con kwashiorkor marásmico tienen todas las características del marasmo nutricional, incluso emaciación grave, falta de grasa subcutánea, crecimiento deficiente, y además del edema, que siempre se encuentra, pueden tener también algunas de las características del kwashiorkor ya descritas. Asimismo puede ocasionar cambios en la piel, por ejemplo, dermatosis en copos de pintura; cambios del cabello, cambios mentales y hepatomegalia. Muchos de estos niños presentan diarrea.
PRUEBAS DE LABORATORIO
Los exámenes de laboratorio tienen una utilidad limitada para el diagnóstico o la evaluación de la MPE. Se utilizan algunas pruebas bioquímicas que dan resultados diferentes en los niños con kwashiorkor y con marasmo nutricional que en los niños normales o en los que tienen MPE moderada.
En el kwashiorkor hay una reducción en las proteínas totales del suero y sobre todo de la fracción albúmina. En el marasmo nutricional la reducción es en general mucho menos marcada. A menudo, debido a las infecciones, la globulina sérica es normal o incluso elevada. La albúmina sérica cae a niveles bajos o muy bajos tan sólo en el kwashiorkor clínicamente evidente. Los niveles de albúmina sérica no son útiles para predecir el desarrollo inminente de kwashiorkor en casos moderados de MPE. Sin embargo, cuanto más grave sea el kwashiorkor, la albúmina sérica será más baja, pero los niveles de albúmina sérica no son útiles para evaluar la MPE menos grave.
Existe un acuerdo general en que las concentraciones de albúmina sérica por debajo de 3 g/dl son bajas y que cifras inferiores a 2,5 g/dl son muy graves (véase el Cuadro 22). Se ha sugerido también que los niveles de albúmina sérica por debajo de 2,8 g/dl se deben considerar anormales e indican un riesgo muy grande.
La determinación de albúmina sérica es relativamente fácil y económica de realizar, y a diferencia de otras pruebas bioquímicas que se mencionan a continuación, se puede hacer en laboratorios modestos de muchos países en desarrollo.
Los niveles de otras dos proteínas séricas, prealbúmina y transferrina sérica, son también de utilidad y fáciles de determinar. Los niveles de ambas se reducen en el kwashiorkor y pueden ser útiles para juzgar su gravedad. El estado del hierro también afecta los niveles de transferrina sérica, lo que disminuye su utilidad como indicadora de kwashiorkor.
Los niveles de proteína ligada al retinol (PLR), que es la proteína que transporta el retinol, también tienden a ser reducidos en el kwashiorkor y en menor grado en el marasmo nutricional. Otras enfermedades, como la enfermedad hepática, las carencias de vitamina A y zinc y el hipertiroidismo, pueden asimismo afectar los niveles de PFR.
CUADRO 22
Niveles de albúmina sérica en niños malnutridos
|
Concentración (g/dl) |
Interpretación |
|
³ 3,5 |
Normal |
|
3-3,4 |
Subnormal |
|
2,5-2,9 |
Baja |
|
£ 2,5 |
Patológica |
Fuente. Alleyne et al., 1977.
Otras pruebas bioquímicas que se han utilizado o que se recomiendan para diagnosticar o evaluar la MPE tienen una utilidad limitada. Estas incluyen pruebas para determinar:
niveles de insulina sérica en ayunas, son altos en el kwashiorkor y bajos en el marasmo;
la relación entre los aminoácidos séricos esenciales y los no esenciales, es baja en el kwashiorkor pero no afecta mucho en el marasmo nutricional;
niveles urinarios de hidroxiprolina y creatinina, si son bajos pueden indicar carencias actuales de crecimiento y marasmo nutricional.
Estas pruebas no son específicas y la mayoría no se pueden hacer en los laboratorios de hospitales comunes.
TRATAMIENTO DE LA MPE
GRAVE
Hospitalización
Si es posible, a todos los niños con kwashiorkor grave, marasmo nutricional o kwashiorkor marásmico, se los deben hospitalizar en compañía de la madre. Al niño se le debe realizar una evaluación clínica completa, que incluya un examen cuidadoso para detectar cualquier infección y en especial buscar alguna infección respiratoria como neumonía o tuberculosis. Se deben hacer exámenes de materia fecal, orina y sangre (para hemoglobina y parásitos de malaria) y medir el peso y la talla del niño.
Muchas veces no es posible el tratamiento hospitalario. En tal caso, se requiere la mejor atención médica disponible que se pueda dar en un centro de salud, dispensario u otra institución de salud. Si el niño aún se alimenta con leche materna, debe continuarse la lactancia.
Alimentación. El tratamiento generalmente se basa en leche en polvo descremada (LPD).[1] La LPD se puede reconstituir fácilmente en el hospital agregando una cucharadita de LPD a 25 ml de agua hervida, mezclando completamente. El niño debe recibir 150 ml de esta mezcla por kilogramo de peso corporal por día, suministrada en 6 comidas, a intervalos de aproximadamente cuatro horas. Por ejemplo, un niño de 5 kilos debe recibir 5 x 150 ml por día = 750 ml por día, dividido en seis comidas = 125 ml por comida. Cada comida debe prepararse agregando cinco cucharaditas de LPD en 125 ml de agua.
La mezcla de leche se debe dar al niño en una taza o con cuchara. Si es difícil alimentarlo con taza o cuchara - lo que puede suceder si el niño no tiene apetito y no es capaz de colaborar, o si el niño está enfermo de gravedad - es mejor suministrar la misma mezcla a través de una sonda gástrica. El tubo debe ser de polietileno, tener alrededor de 50 cm de longitud y un diámetro interno de 1 mm. Se pasa por una fosa nasal hasta el estómago. El extremo exterior se debe asegurar a la mejilla, ya sea con cinta pegante o con pasta de óxido de zinc. La sonda se puede dejar durante cinco días en forma segura. La mezcla de leche se suministra mejor por goteo continuo, como para una transfusión. Como alternativa, la mezcla se puede administrar intermitentemente con una jeringa grande y una aguja que se adapte al tubo. La mezcla de leche se suministra con intervalos de cuatro horas. Antes y después de cada comida se deben inyectar 5 ml de agua tibia, previamente hervida, a través del tubo para evitar que se obstruya.
Existen mezclas mejores que la simple LPD. Todas se pueden administrar exactamente en la misma forma (con cuchara, taza o sonda gástrica). La mayoría de estas mezclas contienen un aceite vegetal (por ejemplo, aceite de sésamo, aceite de semilla de algodón), caseína (proteína pura de leche), leche en polvo descremada y azúcar. Los aceites vegetales aumentan el contenido energético y la densidad energética de la mezcla y parece que se toleran mejor que la grasa de la leche sin descremar. La caseína aumenta el costo de la mezcla, pero como casi siempre sirve para reducir la estadía en el hospital, el dinero está bien invertido. Una buena fórmula y fácil de recordar para la mezcla es azúcar/caseína/aceite/leche (ACAL): una parte de azúcar, una parte de caseína, una parte de aceite y una parte de LPD, más agua para hacer 20 partes. La mezcla seca ACAL se puede conservar hasta un mes en una lata sellada. Para preparar una comida, se coloca la cantidad que se desee de la mezcla en una taza para medir y se agrega agua hasta el nivel correcto. Al revolver, o mejor aún, si se agita con rapidez, se obtiene una mezcla uniforme. Como con la mezcla LPD sola, se debe administrar 150 ml de la mezcla ACAL líquida por kilogramo de peso corporal por día; un niño de 5 kg debe recibir 750 ml por día en seis comidas de 125 ml, cada una de ellas se prepara al añadir cinco cucharaditas de la mezcla ACAL a 125 ml de agua hervida. Una porción de 30 ml en forma líquida suministra alrededor de 28 kcal, 1 g de proteína y 12 mg de potasio.
Rehidratación. Los niños con kwashiorkor o marasmo nutricional que presentan diarrea grave o diarrea con vómito pueden estar deshidratados. La alimentación endovenosa no se requiere a menos que el vómito sea grave o que el niño se niegue a recibir líquidos orales. La rehidratación se debe hacer mediante una solución estándar para rehidratación oral (SRO), como se describe en el tratamiento de la diarrea (véase el Capítulo 37). Para los niños gravemente desnutridos, la SRO mucho más diluida en muchos casos tiene ciertas ventajas terapéuticas. Por lo tanto, si se utilizan los paquetes estándar de SRO, a los que normalmente se les agrega un litro de agua hervida, en un caso serio se puede combinar un paquete con 1,5 litro de agua.
Tratamiento de la hipotermia. Inclusive en áreas tropicales, por la noche a menudo la temperatura desciende bastante en las salas de los hospitales y en otros lugares. Los niños gravemente desnutridos tienen dificultad para mantener su temperatura y pueden fácilmente desarrollar una temperatura corporal por debajo de lo normal, lo que se denomina hipotermia. La hipotermia que no se trata es causa de muerte en niños desnutridos. En su casa el niño puede haberse mantenido caliente al dormir en la cama con la madre, o al tener las ventanas cerradas. En la sala del hospital el niño puede dormir solo y el personal mantener las ventanas abiertas. Si la temperatura del niño está por debajo de 36°C, se debe hacer esfuerzos por calentarlo, mediante atuendo apropiado y ropa de cama abrigada, y asegurarse de que la sala tenga un calor adecuado. Algunas veces se utilizan botellas de agua caliente en la cama. La temperatura del niño se debe vigilar con regularidad.
Medicamentos. Aunque conviene establecer procedimientos estandarizados para tratar el kwashiorkor y el marasmo nutricional en cualquier hospital o centro de salud, sin embargo, se debe manejar cada caso de acuerdo con sus características propias. No hay dos niños con necesidades idénticas.
Las infecciones son tan comunes en los niños gravemente desnutridos que los antibióticos se recomiendan casi siempre de rutina. La penicilina benzatina por inyección intramuscular, 1 millón de unidades diarias, en dosis fraccionadas durante cinco días, se utiliza a menudo para este tratamiento. También se puede suministrar ampicilina, 250 mg en tabletas cuatro veces al día o amoxicilina 125 mg tres veces al día por vía oral. La gentamicina y el cloranfenicol son opciones alternativas pero se utilizan con menos frecuencia.
En áreas endémicas de malaria es recomendable un agente antimalárico, por ejemplo, media tableta (125 mg) de cloroquina diariamente durante tres días, y luego una tableta semanal. En casos graves y cuando hay presencia de vómito, la cloroquina se debe suministrar en inyecciones.
Si la anemia es muy grave se debe tratar mediante transfusión sanguínea y luego continuar con una compuesto de sulfato ferroso o tabletas que se suministran tres veces por día.
Si un examen de materia fecal revela la presencia de uncinaria, áscaris u otros parásitos intestinales, entonces hay que dar un medicamento antihelmíntico como abendazol después que la condición general del niño haya mejorado.
No es raro que los niños gravemente desnutridos tengan tuberculosis, es necesario examinarla para descubrirla. Si se encuentra, hay que aplicar el tratamiento específico.
Recuperación
En el esquema terapéutico descrito anteriormente, un niño con kwashiorkor grave casi siempre empieza a perder edema durante los primeros tres a siete días, con la consecuente pérdida de peso. Durante este período, la diarrea debe mejorar o cesar, el niño debe estar más alegre y alerta, y las lesiones de la piel empiezan a desaparecer.
Cuando se controla la diarrea, el edema desaparece y el apetito regresa, conviene suspender la alimentación por sonda si se ha utilizado este método. Se puede continuar con ACAL o la mezcla única de LPD dando el alimento con taza y cuchara, o en taza. No se debe utilizar el biberón. Si el niño todavía tiene anemia, se debe iniciar un tratamiento con hierro por vía oral y dar media tableta (125 mg) de cloroquina semanalmente.
Los niños con marasmo nutricional grave pueden consumir gran cantidad de energía y el aumento de peso ser bastante rápido. Sin embargo, el tiempo que necesitan estar hospitalizados o para su recuperación total, puede ser mayor que para los niños con kwashiorkor.
En ambas situaciones, mientras sigue la mejoría, casi siempre durante la segunda semana en la clínica, el enfermo aumenta de peso. Mientras se continúa la alimentación con leche, se introduce en forma gradual una dieta mixta, dirigida a suministrar la cantidad de energía, proteína, minerales y vitaminas que el niño necesita.
Para que no haya recaídas, es importante que la madre o la persona que cuida al niño participe en su alimentación durante esta etapa. Se les debe informar sobre todo lo que se le aporta al niño y por qué. Su cooperación y apoyo a este régimen es mucho más probable, si la dieta del niño en el hospital se basa sobre todo en productos de consumo común en el hogar y que son accesibles a la familia. Esto no se puede hacer en todos los casos en un hospital grande, pero la dieta se debe basar, por lo menos, en alimentos disponibles en la localidad. Por ejemplo, en una región donde el maíz es la base de la alimentación, el niño debería recibir papilla de maíz con LPD. A un niño de mayor edad se le puede agregar maní molido dos veces al día, o si se prefiere, de acuerdo con la costumbre, maní tostado. Asimismo se le pueden proporcionar unas cuantas cucharadas de papaya madura, mango, naranja u otra fruta, y una a dos veces al día, pequeñas porciones de hortalizas verdes y fríjoles, pescado o carne bien picados, lo mismo que consume la madre. También se pueden dar alimentos ricos en proteínas (por ejemplo, fríjoles, arvejas, maní, carne, leche agria o huevos). Si hay disponibilidad de huevos y la costumbre permite su consumo, se le puede dar un huevo hervido o revuelto, sería conveniente que la madre observe cuando se prepara. Alternativamente, también se puede agregar un huevo crudo a la papilla a punto de hervir. Los alimentos ricos en proteína de origen animal son a menudo relativamente costosos. Estos no son esenciales; una buena mezcla de cereales, legumbres y hortalizas sirve para el mismo propósito. Si no hay disponibilidad de alimentos que contengan cantidades adecuadas de vitaminas, entonces se debe usar una mezcla de vitaminas, debido a que la LPD y las mezclas de ACAL no son ricas en vitaminas.
La dieta anterior basada en maíz es sólo un ejemplo. Si la dieta de la región se basa en arroz o trigo, éstos se pueden utilizar en vez del maíz. Si el alimento básico es el plátano o la yuca, entonces es importante suministrar suplementos ricos en proteínas.
Una vez que se ha dado de alta, o si se trata de un caso moderado de kwashiorkor atendido en la casa y no en el hospital, si es factible se debe vigilar la salud del niño en una consulta externa o en un centro de salud. Es mucho mejor si estos casos se pueden atender separados de otros enfermos (por ejemplo, una tarde en particular o una sesión de puericultura o de vigilancia del crecimiento) para evitar el tumulto de los horarios de consulta externa. Es importante contar con un ambiente tranquilo y que el personal de salud tenga tiempo para explicarle a la madre los puntos esenciales a fin de asegurarse que entienda lo que se espera de ella. No tiene valor entregar tan sólo una bolsa de leche en polvo u otro suplemento, o simplemente pesar al niño, sin darle a la madre un consejo sencillo pero que sea de utilidad.
El aumento satisfactorio de peso es un buen indicador de progreso. El niño se debe pesar en cada visita y marcar el peso en un cuadro gráfico de crecimiento, a fin de que tanto la madre como el trabajador de salud visualicen la mejoría.
El tratamiento de los pacientes en la consulta externa se debe basar en el suministro de un suplemento dietético apropiado, pero en la mayoría de los casos es mejor que el suplemento sea parte de la alimentación. A la madre se le debe mostrar una cucharita y decirle cuántas por día, según su peso, se le debe dar al niño. Muchos suplementos, y en especial la LPD, se suministran mejor si se agregan a les alimentos habituales del niño (como la papilla de cereal) en vez de hacer una preparación aparte. Se debe preguntar a la madre cuántas veces alimenta al niño en el curso del día. Si lo alimenta sólo a la hora en que come la familia y ésta apenas tiene dos comidas diarias, entonces se le debe enseñar a la madre que es necesario dar dos comidas adicionales al niño.
Si es factible y hay instalaciones adecuadas, la mezcla ACAL se puede utilizar para el tratamiento de pacientes ambulatorios. Es mejor entregarla ya lista en bolsas de polietileno selladas.
PRONÓSTICO
Casi todas las muertes de niños hospitalizados por kwashiorkor o marasmo nutricional tienen lugar durante los tres primeros días después de la admisión. Las tasas de mortalidad dependen de muchos factores, que incluyen la gravedad de la enfermedad del niño en el momento del ingreso y de lo pertinente del tratamiento instaurado. En algunas sociedades los niños enfermos se llevan muy tarde al hospital cuando están casi moribundos. En esta situación las tasas de mortalidad son altas.
La causa y la gravedad de la enfermedad determinan el pronóstico. Un niño con marasmo grave y los pulmones muy afectados por la tuberculosis, obviamente tiene mal pronóstico. Las posibilidades de un niño con marasmo leve y sin ningún otro tipo de infección son mejores. La respuesta al tratamiento quizá es más lenta en el marasmo que en el kwashiorkor.
Con frecuencia, es difícil saber lo que conviene hacer cuando el niño se ha recuperado, sobre todo si es menor de un año de edad. Puede que el niño no tenga madre o que ésta se encuentre enferma, o que la leche materna sea insuficiente o que carezca de ella. Es imprescindible la instrucción y la educación nutricional de la persona responsable del niño. Si a éste lo ha traído el padre, entonces algún pariente femenino debe estar unos cuantos días en el hospital antes que se le dé de alta al niño. Esta persona debe recibir instrucciones sobre cómo alimentarlo con cuchara o taza y se le debe indicar que no alimente al niño con biberón, a no ser que tenga menos de tres meses de edad. El mejor procedimiento es en general suministrarle una papilla poco espesa hecha a partir del alimento básico local, más dos cucharaditas de LPD (o algún otro suplemento rico en proteínas) y dos cucharaditas de aceite por kg de peso corporal diariamente. Si el niño tiene más de seis meses de edad, se deben dar instrucciones sobre los otros componentes que se han de incluir en la dieta. Se debe informar a la madre o a la persona responsable sobre la necesidad de visitar cada semana el hospital o centro de salud, si la familia vive suficientemente cerca (en un radio de 10 km) o a intervalos mensuales si la distancia es mayor. En cada una de las visitas se le debe entregar un suplemento apropiado que debe durarle un poco más que el espacio entre las visitas. El niño puede recibir otros alimentos, como se mencionó en el Capítulo 6 a propósito de la alimentación infantil.
Es esencial que la dieta suministre energía y proteína suficientes. En general, 120 kcal y 3 g de proteína por kg de peso corporal por día, son bastantes para un tratamiento a largo plazo. Por lo tanto, un niño de 10 kg de peso debe recibir aproximadamente 1 200 kcal y 30 g de proteína por día. Debe anotarse que un niño con marasmo, durante la primera fase de la recuperación, es capaz de consumir y utilizar 150 a 200 kcal y 4 a 5 g de proteína por kg de peso corporal diariamente.
MALNUTRICIÓN PROTEINOENERGÉTICA EN
ADULTOS
Kwashiorkor del adulto
No hay dudas que un desorden debido sobre todo a la falta de energía existe también en adultos; es más común en comunidades que sufren de escasez crónica de proteína. El paciente tiene peso muy bajo para su estatura (a menos que tenga edema grave), los músculos están disminuidos y la grasa subcutánea reducida. Son comunes los cambios mentales: el enfermo por lo general no se interesa por nada y parece estar en un mundo de ensueño. Es difícil atraer su atención y también difícil mantenerla, hay fallas en el apetito y el individuo es muy débil.
Casi siempre se puede evidenciar algún grado de edema, que puede ocultar la pérdida de peso, la pérdida de masa muscular y la falta de grasa subcutánea. El edema es más común en las piernas y en los varones también en el escroto, pero puede afectar cualquier parte del cuerpo. No es raro que la cara esté hinchada. Esta condición se ha denominado «edema de hambre» debido a que tiene lugar donde hay inanición resultante de hambrunas u otras causas. Se informó que fue común en las hambrunas de Indonesia y Papua Nueva Guinea.
A menudo aparece diarrea fétida. El abdomen está ligeramente distendido, y a la palpación los órganos se pueden sentir con facilidad a través de la delgada pared abdominal. Durante la palpación casi siempre se perciben borborigmos en el abdomen, y se pueden sentir movimientos peristálticos con la punta de los dedos. No es raro que los pacientes adultos con kwashiorkor consideren su estado físico consecuencia del trastorno abdominal. Por este motivo, algunas veces utilizan purgantes fuertes, basados en hierbas o productos de marca, y enemas picantes antes de ir al hospital, lo que puede en gran parte agravar la situación.
A menudo hay cambios en el cabello y la piel está seca y escamosa con apariencia de pavimento errático, especialmente sobre la tibia. Es común la hinchazón de ambas parótidas y al palparlas muestran consistencia firme y elástica.
Casi siempre se presenta anemia que puede ser grave. La presión arterial es baja. Por lo general, sólo hay huellas de albúmina en la orina.
El edema también se puede deber a la anemia grave. En los adultos con MPE existe menos disnea que en la anemia y generalmente no hay cardiomegalia. Otras características como los cambios del cabello y la inflamación de las parótidas son comunes en la MPE de adultos pero no en la anemia. Sin embargo, los dos estados se relacionan íntimamente.
Marasmo nutricional en adultos
En contraste con el kwashiorkor de los adultos o el edema causado por hambruna que son poco predominantes, el equivalente del marasmo nutricional en los adultos es muy común. Las cinco causas principales son las siguientes.
Falta de alimentos. Cualquier niño mayor o persona adulta cuya dieta sea muy deficiente en energía desarrollará signos casi exactamente iguales a los del marasmo nutricional, y si la enfermedad progresa puede con frecuencia llegar a ser fatal. En el caso de las hambrunas, la condición se puede denominar inanición (véase el Capítulo 24). Las hambrunas y la ausencia grave de alimentos como consecuencia de guerra, disturbios civiles o desastres naturales (sequías, inundaciones y terremotos), pueden ocasionar marasmo nutricional en los niños y un estado similar en los adultos, que ocasiona pérdida de peso, emaciación, diarrea, infecciones, etc.
Infecciones. La segunda causa principal de emaciación grave o de MPE grave en los adultos son las infecciones, sobre todo las infecciones crónicas no tratadas o que son intratables. De éstas, la más común ahora es el síndrome de inmunodeficiencia adquirida (SIDA) que resulta de la infección con el virus humano de inmunodeficiencia (VHI). A medida que la enfermedad progresa se produce una gran pérdida de peso y emaciación grave. Como se mencionó en el Capítulo 3, en Uganda se le ha dado al SIDA el nombre «enfermedad del enflaquecimiento» debido a la delgadez de sus víctimas. La tuberculosis avanzada y muchas otras infecciones crónicas de largo plazo también ocasionan emaciación y pérdida de peso.
Malabsorción. Varios estados de malabsorción ocasionan MPE en adultos y niños. Estas enfermedades, algunas hereditarias, son el resultado de la incapacidad del cuerpo para digerir o absorber ciertos alimentos o nutrientes. Ejemplos son la fibrosis cística, la enfermedad celíaca y el esprue del adulto.
Neoplasias. Otra causa de emaciación en personas de cualquier edad son los procesos malignos o cáncer de cualquier órgano, una vez que progresa hasta un estado intratable por resección quirúrgica. La caquexia es una característica de muchos cánceres avanzados.
Desórdenes alimentarios. Varios trastornos en la alimentación ocasionan pérdida de peso que conduce al equivalente de la MPE. La que se describe con más amplitud es la anorexia nerviosa, que es más frecuente en mujeres que en varones, en adolescentes o adultos jóvenes que en personas de mayor edad, y en sociedades ricas que en las pobres. Otras condiciones psicológicas pueden también ocasionar un consumo deficiente de alimentos y llevar a la MPE.
Tratamiento
El tratamiento de la MPE en adultos incluye el manejo de la causa subyacente de la enfermedad y la terapia relacionada con la alimentación y la rehabilitación, cuando tal causa lo permita. Por lo tanto, infecciones como la tuberculosis o la amibiasis crónica, necesitan una conducta específica que cuando es efectiva eliminará el origen de la pérdida de peso y la emaciación. Por el contrario, el tratamiento curativo no es aplicable en casos avanzados de SIDA o de cáncer.
El tratamiento dietético para la MPE del adulto se debe basar en principios semejantes a los descritos para el manejo de la MPE grave en niños, incluyendo los que se recuperan de kwashiorkor o marasmo. La alimentación de emergencia y la rehabilitación de las víctimas de hambruna (descritas en Capítulo 24) se aplica también en la MPE de los adultos.
PREVENCIÓN Y CONTROL DE LA MPE
La prevención de la MPE es un reto enorme en Asia, África y el continente americano. Es mucho más difícil de controlar, que por ejemplo los trastornos por carencia de yodo (TCY) y la carencia de vitamina A, debido a las causas subyacentes y básicas que, como se mencionó antes, son a menudo numerosas y complejas, y porque no existe una sola estrategia sencilla, universal y económica, que pueda aplicarse en todas partes para reducir la prevalencia o gravedad de la MPE.
La Parte V de este libro incluye varias estrategias para reducir la prevalencia de la MPE. Se sugieren políticas y programas apropiadas de nutrición, y en capítulos separados se trata, por ejemplo la forma de mejorar la seguridad alimentaria, cómo proteger y promover la buena salud, y las prácticas correctas para garantizar una buena nutrición. Estos capítulos proporcionan guías sobre cómo tratar las tres causas subyacentes de la malnutrición: alimentación, salud y cuidados inadecuados, que en el Capítulo 1 se incluyen en el marco conceptual de referencia para la malnutrición. Otros capítulos en la Parte V discuten soluciones de aspectos particulares del problema, incluyendo el mejoramiento de la calidad y seguridad de los alimentos, la promoción de dietas apropiadas y estilos de vida saludable, distintas formas de obtener alimentos e incorporación de objetivos nutricionales en las políticas y programas de desarrollo. La Parte V, en su totalidad, da énfasis a mejorar la calidad de vida de las personas, de modo especial a los esfuerzos para reducir la pobreza, mejorar la alimentación y difundir la buena salud. Es fundamental intensificar el consumo de energía de las personas expuestas al riesgo de la MPE.
A finales de la década de 1950 y durante la de 1960 se pensó que buena parte de la MPE se debía principalmente al poco consumo de proteína. Entonces se dio gran énfasis a los alimentos ricos en proteína como una solución importante al enorme problema de la malnutrición en el mundo. Esta estrategia, poco apropiada, desvió la atención de la necesidad primordial que es el consumo adecuado de alimentos por parte de los niños. Ahora se da mucho menos énfasis a los alimentos con alto contenido proteico para el destete como también a los esfuerzos de educación nutricional para asegurar un mayor consumo de carne, pescado y huevos, ya que ambas situaciones están económicamente fuera del alcance de muchas familias que tienen niños con MPE.
La proteína es un nutriente esencial, pero la MPE se asocia más a menudo con fallas en el consumo alimentario que con deficiencia en la ingestión de proteína. En general, cuando las dietas basadas en cereales de uso común cumplen con las necesidades energéticas, también cumplen con las necesidades de proteína, sobre todo si la dieta además suministra algunas cantidades de legumbres y hortalizas. Es necesario prestar atención al aumento de la ingestión de alimentos y a la reducción de las infecciones.
Se requieren grandes esfuerzos para proteger y promover la lactancia y el destete apropiados; para que los niños menores de un año incrementen el consumo de cereales, legumbres y otros alimentos para el destete producidos localmente; para prevenir y controlar las enfermedades infecciosas y parasitarias; para aumentar la frecuencia de las comidas de los niños y, donde sea posible, estimular un consumo mayor de aceite, grasa y otros productos que reducen el volumen y aumentan la densidad energética de los alimentos que reciben los niños expuestos a riesgo. Es probable que estas medidas tengan más impacto si se acompañan de un control del crecimiento, vacunaciones, terapia de rehidratación oral para la diarrea, manejo precoz y preciso de enfermedades comunes, desparasitación periódica y atención a las causas subyacentes de la MPE, como la pobreza y la desigualdad. Algunas de estas medidas se pueden llevar a cabo como parte de la atención primaria de salud. Los lectores que planifiquen estrategias para controlar la MPE deben consultar la Parte V de esta publicación.
FOTO 15
Marasmo nutricional con emaciación extrema en un niño de Rotterdam,
Holanda, durante la segunda guerra mundial
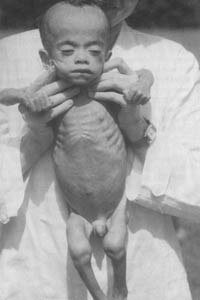
FOTO 16
Un niño con kwashiorkor muestra dermatosis del muslo, brazo y espalda;
el edema de piernas y cara encubre la emaciación y la falta de crecimiento
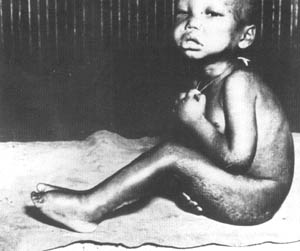
FOTO 17
Edema, cambios en la piel y una úlcera cerca del codo que se ven en el
kwashiorkor
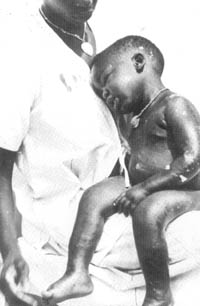
FOTO 18
Un niño colombiano con marasmo nutricional
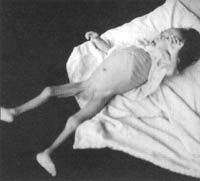
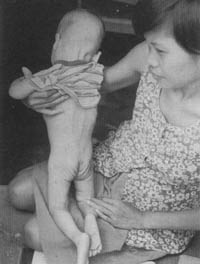
FOTO 19
Evidente pérdida de grasa subcutánea en un niño con marasmo
nutricional de las filipinas
| [1] Existe
el riesgo si se utiliza LPD sin fortificar. Es importante prestar atención
al suministro de todos los micronutrientes. |