La malnutrition protéino-énergétique (MPE) du jeune enfant est actuellement le problème nutritionnel le plus grave dans de nombreux pays en Asie, en Amérique latine, au Proche-Orient et en Afrique. Un déficit calorique en est la cause principale. On ne dispose pas de données précises sur sa prévalence dans le monde, mais les estimations de l'OMS suggèrent que la MPE serait passée de 42,6 pour cent des enfants de moins de 5 ans en 1975 à 34,6 pour cent en 1995. Cependant, dans certaines régions, ce déclin a été moins rapide que l'accroissement de la population, si bien que dans certaines zones d'Afrique et d'Asie du Sud, le nombre d'enfants souffrant de MPE a augmenté en valeur absolue. Dans le monde entier, le nombre d'enfants de faible poids est passé de 195 millions en 1975 à environ 200 millions fin 1994, soit plus d'un tiers de la population des enfants de moins de 5 ans.
Le retard de croissance est le premier symptôme important de MPE. Il est habituellement dû à une consommation insuffisante d'aliments et de calories, et il est aggravé par les infections. Un enfant qui souffre d'un retard de croissance peut être plus petit ou plus léger qu'il ne devrait l'être à son âge, ou trop maigre pour sa taille.
Le cadre conceptuel exposé au chapitre 1 suggère que trois conditions sont nécessaires pour éviter la malnutrition et le retard de croissance: disponibilité et consommation suffisantes d'aliments; bonne santé et accès aux soins; soins appropriés et bonnes habitudes alimentaires dans la famille. Si l'une de ces conditions fait défaut, une MPE a des chances de survenir.
Bien que le terme de MPE soit récent, le problème, lui, est connu depuis longtemps. On l'appelait auparavant "malnutrition protéinocalorique" et "déficit protéinoénergétique".
Le terme MPE recouvre en fait un ensemble d'états cliniques allant des plus bénins aux plus graves. Une malnutrition modérée se traduit simplement par une croissance médiocre, alors que les formes les plus graves, le kwashiorkor (accompagné d'œdèmes) et le marasme nutritionnel (amaigrissement majeur), sont souvent mortelles.
On sait depuis longtemps qu'un apport alimentaire très insuffisant (famine ou pénurie) entraîne un amaigrissement pouvant aboutir au décès par épuisement. Mais ce n'est qu'en 1930 que Cicely Williams, qui travaillait au Ghana, a décrit en détail une maladie qu'elle a appelée de son nom local, "kwashiorkor", qui signifie "maladie de l'enfant déplacé". Le kwashiorkor a fait l'objet d'une grande attention à partir des années 50. Il était décrit comme la forme majeure de malnutrition et on le croyait dû à un déficit protéique. On a donc pensé que la solution consistait à augmenter les rations d'aliments riches en protéines pour les enfants à risque, et on relègue au deuxième plan le problème du marasme et du déficit énergétique. Actuellement, on pense que la MPE résulte d'un apport alimentaire insuffisant ou d'une mauvaise utilisation des aliments et non d'un déficit d'un nutriment particulier comme les protéines. On a aussi constaté progressivement le rôle majeur des infections. On sait maintenant que le marasme est souvent plus fréquent que le kwashiorkor, mais on ne sait pas pourquoi un enfant souffre plutôt d'un syndrome que de l'autre. Par ailleurs, on a pris conscience que ces deux formes cliniques graves ne constituent que la partie émergée de l'iceberg. Dans la majorité des pays pauvres, la prévalence ponctuelle du kwashiorkor et du marasme réunis est de 1 à 5 pour cent, alors que 30 à 70 pour cent des enfants de moins de 5 ans souffrent de malnutrition bénigne ou modérée diagnostiquée par anthropométrie.
La malnutrition protéino-énergétique résulte d'un déficit en macronutriments et non en micronutriments. Malgré son appellation, on admet à présent qu'elle provient avant tout d'un déficit calorique dû à un apport alimentaire insuffisant. Le déficit calorique est plus fréquent et plus important que le déficit protéique. La MPE est très souvent associée à des infections et à des déficits en micronutriments. Des soins insuffisants, comme des repas trop peu fréquents, jouent également un rôle.
Il ne faut cependant pas limiter les causes de la MPE et autres déficits courants dans les pays en développement à un apport alimentaire insuffisant. Pour que la nutrition soit satisfaisante, plusieurs conditions doivent être remplies: les aliments doivent être accessibles à la famille en quantité correcte; l'enfant doit recevoir plusieurs repas équilibrés à intervalles adéquats; il doit avoir de l'appétit; la digestion et l'absorption des aliments doivent être bonnes; le métabolisme doit être normal; et il ne doit pas y avoir de problème qui empêche les cellules d'utiliser ces nutriments ou qui entraîne des pertes anormales. Tout facteur entravant les conditions précitées peut induire une malnutrition, notamment une MPE. L'étiologie peut être complexe, car certains des facteurs contribuant à une MPE, surtout chez le jeune enfant, sont liés à la fois à l'hôte, à l'agent (l'alimentation) et au milieu ambiant. On peut également classer les causes sous-jacentes selon qu'elles sont liées à la sécurité alimentaire, à la santé (y compris la protection vis-à-vis des infections et le traitement des maladies) ou aux soins (y compris les habitudes maternelles et familiales en matière d'allaitement, de sevrage et de fréquence des repas).
Voici quelques facteurs contribuant à la MPE:
La prématurité ou un petit poids de naissance prédisposent au marasme. L'absence d'allaitement due au décès de la mère, une séparation d'avec la mère, un lait maternel absent ou insuffisant peuvent également déclencher une malnutrition dans des sociétés pauvres où l'allaitement maternel est la seule façon de nourrir les bébés correctement. Tout ce qui empêche une mère d'allaiter son enfant dans une famille où l'utilisation du biberon serait difficile, voire dangereuse, peut conduire à la malnutrition. Ce peut être la publicité en faveur des laits en poudre comme le manque de soutien de l'allaitement par les professionnels de santé. Par contre, l'allaitement exclusif sans adjonction d'autres aliments après l'âge de 6 mois peut lui aussi empêcher une croissance correcte et aboutir à un kwashiorkor ou à un marasme.
Le concept selon lequel le kwashiorkor résulte d'un déficit protéique, et le marasme d'un déficit calorique, est simpliste car les causes en sont bien plus complexes. Des causes endogènes et exogènes font qu'un enfant va souffrir de kwashiorkor, de marasme, ou de cet état intermédiaire appelé "kwashiorkor marastique". Si un enfant consomme beaucoup moins d'aliments qu'il ne faut, il tire son énergie de ses graisses de réserve et de ses muscles. La néoglucogénèse hépatique s'accélère et la graisse sous-cutanée et les muscles fondent. On a émis l'idée que, dans ce contexte, surtout si l'apport protéique est très faible par rapport à l'apport glucidique (phénomène aggravé par des pertes azotées liées aux infections), diverses modifications métaboliques surviennent et contribuent à l'apparition des œdèmes. L'eau et le sodium sont retenus et se combinent en dehors du système cardiovasculaire dans les tissus, créant des œdèmes. Le véritable rôle des infections n'a pas été totalement élucidé, mais on sait que certaines infections augmentent considérablement l'élimination d'azote urinaire dérivé des acides aminés des muscles.
Il n'y a pas encore de consensus sur la véritable cause des œdèmes caractéristiques du kwashiorkor. La majorité des chercheurs s'accorde sur l'importance du déficit en potassium et de la rétention de sodium. Quelques éléments étayent l'argument classique selon lequel les œdèmes sont un signe d'apport protéique insuffisant. Il est possible, par exemple, d'induire un état similaire au kwashiorkor avec une stéatose hépatique et des œdèmes chez des porcs et des babouins dont l'apport alimentaire est déficient en protéines. Des arguments épidémiologiques montrent aussi que le kwashiorkor est plus fréquent en Ouganda, où le plat de base est la banane plantain, pauvre en protéines, que dans des régions voisines où l'aliment de base est une céréale.
Deux nouvelles hypothèses ont été avancées récemment. La première attribue le kwashiorkor à un empoisonnement par une aflatoxine. La seconde met l'accent sur l'importance des radicaux libres dans sa pathogénèse; on a imaginé que la plupart des signes cliniques du kwashiorkor pourraient être dus à un excès de stress générateur de radicaux libres. Cette théorie nouvelle, qui n'a pas encore fait l'objet de vérifications approfondies, suggère toutefois que, même si le kwashiorkor est dû aux radicaux libres, il ne survient que chez des enfants mal nourris et sujets aux infections. Même si cette théorie est vérifiée, elle ne ferait qu'expliquer l'un des mécanismes pathogènes du kwashiorkor. Elle ne changerait rien au fait que seuls l'amélioration de l'apport alimentaire et la lutte contre les infections permettent de réduire significativement le kwashiorkor et le marasme. Ni la théorie de l'aflatoxine ni celle des radicaux libres n'ont été expérimentalement prouvées et il n'y a pas d'arguments convaincants en faveur de l'hypothèse d'une inadaptation individuelle à l'origine d'une MPE grave. Il est étonnant qu'aucune étude n'ait pu mettre en évidence de différences ou de similitudes de l'apport alimentaire entre les enfants atteints de kwashiorkor et ceux atteints de marasme sans œdème.
Dans les kwashiorkors graves, il y a habituellement des signes biochimiques et souvent cliniques de déficits en micronutriments, ce qui n'est pas surprenant chez un enfant mal nourri. Dans le kwashiorkor comme dans le marasme, et même dans la MPE modérée, l'examen clinique et les tests de laboratoire montrent des signes évidents de déficit, qu'il s'agisse de vitamine A, de fer et/ou de zinc. Par contre, on n'a guère de preuves de la responsabilité de l'un de ces déficits dans la genèse de la MPE ou même des œdèmes.
Quelle que soit la véritable étiologie de la MPE, il faut, pour la prévenir, à la fois augmenter la quantité de l'apport alimentaire, assurer l'équilibre de l'alimentation et lutter contre les infections.
La MPE est souvent comparée à un iceberg dont seuls 20 pour cent sont émergés. La partie émergée correspond aux formes graves: kwashiorkor, marasme et kwashiorkor marastique. Leur diagnostic clinique est relativement facile. Par contre, les enfants souffrant de malnutrition modérée ou bénigne n'ont pas de signes cliniques évidents de malnutrition; ils sont souvent plus petits ou plus maigres, ils ont parfois un retard de développement psychologique ou d'autres signes plus difficiles à détecter. Ces formes de malnutrition ne sont décelées que par anthropométrie, c'est-à-dire mesure de la taille, du poids, et souvent du périmètre brachial et de l'épaisseur du pli cutané.
Comme le montre la figure 5, la prévalence de la malnutrition hautement visible et avancée (kwashiorkor, marasme et kwashiorkor marastique) est de 1 à 5 pour cent sauf dans les zones de famine. La malnutrition modérée et bénigne atteint 30 à 70 pour cent en Afrique subsaharienne et en Asie du Sud-Est. Souvent dans ces régions, seuls 15 à 50 pour cent des enfants de 6 mois à 5 ans n'ont pas de MPE. Le diagramme montre que les déficits protéique et calorique jouent un rôle, mais celui du déficit calorique est plus important. Le déficit protéique est prépondérant dans le kwashiorkor et le déficit calorique dans le marasme. La proportion d'enfants dans chaque catégorie de malnutrition dépend bien sûr de la façon dont ces catégories sont définies. Les deux formes graves ont des signes cliniques très différents: on admet généralement que le trait dominant du kwashiorkor est l'œdème alors que celui du marasme est l'amaigrissement extrême. Quand ces deux signes sont présents, il s'agit d'un kwashiorkor marastique.
La classification dite de Wellcome des formes graves de MPE a été largement utilisée pendant plus de 20 ans (voir tableau 19). Elle a le mérite de la simplicité car elle est basée sur deux mesures seulement: le pourcentage du poids standard pour l'âge et la présence ou non d'œdèmes. La catégorie "mal nourris" inclut tous les enfants qui ont une MPE modérée ou modérément grave mais sans œdèmes et dont le poids est au moins de 60 pour cent du poids standard pour l'âge. Actuellement, on préfère utiliser les écarts types pour déterminer les seuils, mais cela ne modifie pas beaucoup la classification.
Dans les années 50 et 60, l'évaluation du degré de malnutrition était basée presque exclusivement sur le pourcentage du poids standard pour l'âge. En Amérique latine notamment, on utilisait la classification de Gomez (tableau 20).

Au début des années 70, des professionnels de la nutrition se sont mis à signaler les inconvénients du recours exclusif au poids pour l'âge. Une autre méthode a alors été mise au point pour classer les malnutritions légères et modérées en fonction du poids et de la taille. Par la suite, trois catégories ont été définies:
Cette classification distingue les influences passées et présentes sur l'état nutritionnel. Elle permet de déterminer si une supplémentation nutritionnelle a des chances d'améliorer sensiblement l'état de l'enfant et renseigne le praticien sur l'histoire de la malnutrition du patient. Elle est aussi pratique pour les enquêtes et la surveillance nutritionnelles. D'une manière générale, le retard de croissance est plus répandu que l'amaigrissement dans le monde.
TABLEAU 19
Classification de Wellcome des formes graves de MPE
Pourcentage du poids standard pour l'âge |
œdèmes |
Pas d'œdèmes |
60-80 |
Kwashiorkor |
Malnutrition |
< 60 |
Kwashiorkor marastique |
Marasme nutritionnel |
TABLEAU 20
Classification de Gomez de la malnutrition basée sur le rapport poids/âge
Classification |
Pourcentage du poids standard pour l'âge |
Normal |
> 90 |
Premier degré (malnutrition bénigne) |
75-89,9 |
Deuxième degré (malnutrition modérée) |
60-74,9 |
Troisième degré (malnutrition avancée) |
< 60 |
Comme on l'explique au chapitre 33, qui traite de l'évaluation du statut nutritionnel, on recommande actuellement de déterminer le degré de malnutrition en fonction des écarts types par rapport aux courbes de croissance du Centre national des statistiques de santé des Etats-Unis (NCHS), qui sont publiées par l'OMS. Dans les rapports publiés par les pays qui sont basés uniquement sur le rapport poids/âge, on utilise le terme de "maigre" pour parler des enfants dont le poids est inférieur à moins deux écarts types des normes du NCHS pour les enfants de moins de 5 ans. Dans une population normale, il n'y a que 2 à 3 pour cent des enfants à être en dessous de ce seuil. Une prévalence plus élevée est un indice de problème nutritionnel. Si on mesure également la taille des enfants, on peut affiner la classification et distinguer ceux qui sont amaigris, ceux qui ont un retard de croissance ou les deux à la fois.
Il revient aux décideurs et au personnel de santé de définir les critères de croissance en fonction desquels estimer la malnutrition, réaliser des enquêtes et mettre en place une surveillance. Ces dernières années, les normes OMS/NCHS ont été de plus en plus largement adoptées bien qu'elles ne diffèrent pas tellement des précédentes normes de Harvard et de Denver. On a constaté que ces normes internationales s'appliquaient aux enfants des pays en développement puisque la croissance des enfants privilégiés dans ces pays ne s'en écarte pas sensiblement et que la croissance médiocre des enfants défavorisés tient bien davantage à des facteurs sociaux, notamment le cycle infection-malnutrition, qu'à des différences ethniques ou géographiques.
L'importance fonctionnelle d'une malnutrition bénigne ou modérée n'est pas encore totalement élucidée. Des études réalisées dans différents pays montrent que la mortalité croît de façon régulière avec la dégradation du statut nutritionnel. Des enquêtes effectuées chez des adolescents du Guatemala ont montré que ceux qui avaient eu un retard de croissance dans leur petite enfance, étaient plus petits, avaient de moins bons résultats scolaires et que leurs performances physiques et leurs tests de développement psychologique étaient moins bons que ceux des enfants des mêmes villages ayant eu une croissance satisfaisante dans leurs premières années. Ces résultats donnent à penser qu'une MPE précoce a des conséquences négatives à long terme.
La lutte contre la MPE est au cœur des politiques et programmes nutritionnels de la plupart des pays en développement. La réduction, et si possible la prévention, des malnutritions bénignes et modérées diminuera ipso facto les malnutritions graves. C'est pourquoi, et bien qu'il puisse être tentant, en particulier pour le corps médical, de mettre l'accent sur le marasme et le kwashiorkor, il est souvent plus judicieux de consacrer les ressources disponibles à lutter contre les formes modérées de malnutrition qui réduiront à leur tour les formes graves.
Le kwashiorkor est l'une des formes graves de MPE. Il affecte surtout les enfants de 1 à 3 ans, mais on le voit à tout âge. L'alimentation de ces enfants est carencée en énergie, en protéines et en autres nutriments. Elle consiste souvent en glucides qui peuvent être volumineux et ne sont pas offerts à l'enfant assez fréquemment. Le kwashiorkor est souvent associé à, ou déclenché par des maladies infectieuses comme la diarrhée, les infections respiratoires, la rougeole, la coqueluche ou les parasitoses intestinales. Ces infections entraînent une perte d'appétit qui contribue à précipiter l'enfant vers une forme grave de malnutrition. D'autre part, les infections, notamment accompagnées de fièvre, augmentent les pertes azotées qui ne peuvent être compensées que par des protéines alimentaires.
Le diagnostic de kwashiorkor repose sur l'histoire de l'enfant, les symptômes rapportés et les signes cliniques observés (figure 6). Les examens biologiques ne sont pas indispensables mais contribuent à éclairer les cas individuels. Dans tous les cas, il existe des œdèmes à des degrés divers, un retard de croissance, une fonte musculaire et une infiltration graisseuse du foie. On peut aussi voir des modifications du comportement, des anomalies des cheveux, une dermatose typique, une anémie, une diarrhée et divers signes de carences en autres micronutriments (photos 16 et 17).
œdèmes. L'accumulation de liquide dans les tissus entraîne un gonflement qui existe dans tout kwashiorkor à des degrés divers. Cela commence par un léger gonflement des pieds qui remonte le long des jambes et peut ensuite toucher les mains ou la tête. Pour vérifier la présence d'œdème, l'infirmier doit appuyer avec son pouce ou un autre doigt au-dessus de la cheville. En cas d'œdème, le creux qui se forme va mettre quelques secondes à disparaître.
Retard de croissance. C'est un signe constant. Si on connaît l'âge précis de l'enfant, on constatera qu'il est plus petit qu'il ne devrait être et, sauf s'il a des œdèmes très importants, plus léger (en général, 60 à 80 pour cent du poids normal ou inférieur à moins de 2 écarts types). Ce retard peut passer inaperçu si les œdèmes sont importants ou si l'on ignore l'âge de l'enfant.
Amaigrissement. La fonte musculaire est typique mais peut également être masquée par les œdèmes. Cependant, les bras sont presque toujours maigres.
Stéatose du foie. Ce signe est découvert lors de toute autopsie de kwashiorkor. Il peut se traduire par une augmentation de volume palpable du foie (hépatomégalie).
Modifications du comportement. Ces troubles sont fréquents mais pas systématiques. L'enfant est habituellement apathique, ne manifeste pas d'intérêt pour son environnement mais devient irritable si on le dérange ou si on le déplace. Il reste dans la même position, a l'air malheureux et ne sourit pas. Son appétit est toujours médiocre.

Altérations des cheveux. Les cheveux d'un enfant asiatique, sud-américain ou africain sont habituellement noirs et épais et reflètent la lumière. En cas de kwashiorkor, les cheveux deviennent plus soyeux et plus fins. Les cheveux africains se défrisent. La brillance disparaît, la chevelure devient terne et sans ressort et se décolore souvent en brun plus ou moins roux. On peut facilement et sans douleur en arracher de petites touffes. Au microscope, ces touffes ont des altérations des racines et sont plus fines que la normale. Leur résistance à la traction est diminuée. En Amérique latine, on voit des bandes de décoloration (correspondant aux périodes de malnutrition successives) qui ont été appelées le "signe du drapeau" (signo de la bandera).
Altérations cutanées. Les dermatoses ne sont pas constantes. Elles surviennent d'abord dans les zones de frottement ou de pression comme le périnée, les creux poplités et les coudes. On voit apparaître des taches hyperpigmentées qui peuvent desquamer et qui ressemblent à une vieille peinture cloquée par le soleil, d'où leur nom de "dermatose écailleuse". En dessous de ces écailles, la peau est dépigmentée et atrophique comme une cicatrice de brûlure.
Anémie. Une anémie est presque toujours présente en raison du manque de protéines nécessaires à la synthèse des globules sanguins, et elle est souvent majorée par un manque de fer, une ankylostomiase, une infestation palustre, etc.
Diarrhée. Les selles sont habituellement molles et contiennent des aliments non digérés. Elles ont quelquefois une odeur très prononcée, elles peuvent être aqueuses ou striées de sang.
Visage lunaire. Cet aspect caractéristique est dû au gonflement des joues soit par l'œdème soit par une infiltration graisseuse.
Signes liés à d'autres déficits. La quantité de graisse sous-cutanée résiduelle donne une idée du degré de déficit en énergie. On voit souvent des altérations de la bouche et des lèvres typiques des carences en vitamines B, parfois une xérophtalmie témoignant d'une carence en vitamine A ou des signes de déficit en zinc ou autres micronutriments.
Syndrome néphrotique. La confusion est possible puisque, dans les deux cas, il existe des œdèmes. Mais dans le syndrome néphrotique, l'urine contient beaucoup d'albumine ainsi que des débris. Dans le kwashiorkor, il y a au plus des traces d'albumine. Le diagnostic repose sur la dermatose et les autres signes. Enfin, l'ascite fréquente dans le syndrome néphrotique est rare dans le kwashiorkor et ce dernier est une cause beaucoup plus courante d'œdèmes dans les pays en développement.
Anémie grave due à une ankylostomiase. L'anémie peut suffire à expliquer l'œdème, mais elle s'associe souvent au kwashiorkor. Si l'anémie est isolée, il n'y a pas d'autres signes cutanés que la pâleur. De toutes façons, il est toujours utile de vérifier les selles.
Dysenterie chronique. Il n'y a pas d'œdème.
Pellagre. Elle est rare chez le jeune enfant. Les lésions cutanées peuvent ressembler à celles du kwashiorkor, mais elles affectent surtout des zones exposées au soleil, pas le périnée par exemple. La pellagre comporte une diarrhée et une perte de poids mais pas d'œdème ni d'altérations des cheveux.
Dans la majorité des pays, le marasme, deuxième forme grave de MPE, est maintenant beaucoup plus répandu que le kwashiorkor. Le marasme est lié à un déficit de nourriture en général, donc d'énergie. Il peut survenir à tout âge jusque vers 3 1/2 ans mais, contrairement au kwashiorkor, il est plus fréquent avant l'âge de 1 an. Le marasme est une forme de famine et ses causes sont innombrables. Quelle qu'en soit la raison, l'enfant ne reçoit pas suffisamment de lait maternel ou d'un substitut adapté.
Les maladies infectieuses et parasitaires sont les facteurs déclenchants les plus fréquents: rougeole, coqueluche, diarrhée, paludisme et diverses parasitoses, de même que les infections chroniques comme la tuberculose. La prématurité, le retard mental et les troubles digestifs comme les vomissements ou une malabsorption, ainsi que l'interruption de l'allaitement, constituent d'autres causes habituelles.
TABLEAU 21
Comparaison des aspects cliniques du kwashiorkor et du marasme
Caractéristique |
Kwashiorkor |
Marasme |
Retard de croissance |
Présent |
Présent |
Amaigrissement |
Présent |
Marqué |
œdèmes |
Présents (parfois modérés) |
Absents |
Altérations des cheveux |
Fréquentes |
Moins fréquentes |
Troubles du comportement |
Très fréquents |
Rares |
Dermatose écailleuse |
Habituelle |
Non présente |
Appétit |
Médiocre |
Normal |
Anémie |
Parfois grave |
Modérée |
Graisse sous-cutanée |
Diminuée mais présente |
Absente |
Visage |
Parfois _dématié |
Emacié, simiesque |
Infiltration graisseuse du foie |
Présente |
Absente |
Le tableau 21 compare les aspects cliniques du kwashiorkor et du marasme. Voici les principaux signes du marasme (photos 18 et 19)
Retard de croissance. Dans tous les cas, l'enfant ne grandit pas normalement. Le poids est toujours très faible pour l'âge quand ce dernier est connu (inférieur à 60 pour cent moins 3 écarts types de la moyenne). Dans les cas graves, la fonte musculaire est évidente: les côtes sont saillantes, le visage a un aspect simiesque caractéristique; les membres sont très émaciés; le ventre, lui, est souvent ballonné. L'enfant semble n'avoir plus que la peau sur les os. A un stade avancé, on ne peut pas ne pas le reconnaître, et une fois qu'on l'a vu, on ne peut plus l'oublier.
Amaigrissement. La fonte musculaire est extrême et il n'y a plus - ou si peu - de graisse sous-cutanée. La peau est flasque et plissée, surtout au niveau des fesses et des cuisses. En pinçant la peau entre deux doigts, on ne trouve plus de couche de graisse sous-cutanée.
Vivacité. Ces enfants ne sont pas apathiques comme ceux atteints de kwashiorkor. Au contraire, leurs yeux enfoncés ont une apparence éveillée et ils ont souvent l'air moins malheureux et moins irritables.
Appétit. L'appétit est conservé, voire féroce. Ces enfants sucent souvent leurs doigts, leurs vêtements ou n'importe quoi en faisant des bruits de succion.
Anorexie. Quelques enfants sont anorexiques.
Diarrhée. Les selles sont parfois molles, mais ce n'est pas constant. Une diarrhée infectieuse précipite souvent l'évolution vers le marasme.
Anémie. Une anémie est habituelle.
Ulcères cutanés. Il peut y avoir des ulcérations cutanées en regard des os les plus saillants. Mais il n'y a ni œdème, ni dermatose écailleuse.
Altérations des cheveux. Il peut y avoir des altérations similaires à celles du kwashiorkor mais il y a plus souvent une modification de la texture que de la couleur des cheveux.
Déshydratation. Bien que ce ne soit pas vraiment un signe du marasme, la déshydratation l'accompagne souvent. Elle résulte d'une diarrhée grave et/ou de vomissements.
Le diagnostic de kwashiorkor marastique s'applique aux enfants qui présentent des traits des deux affections. Dans la classification de Wellcome, ce terme s'applique aux enfants atteints de malnutrition grave, présentant à la fois des œdèmes et un poids pour l'âge inférieur à 60 pour cent. Ces enfants présentent tous les signes de marasme, notamment l'amaigrissement, la disparition de la graisse sous-cutanée et le retard de croissance, et, en plus des œdèmes constamment présents, ils peuvent avoir différents signes de kwashiorkor comme la dermatose écailleuse, les altérations des cheveux, les troubles du comportement et l'hépatomégalie. La diarrhée est très fréquente.
L'intérêt des examens biologiques dans le diagnostic ou l'évaluation de la MPE est limité. Quelques dosages biochimiques sont altérés dans les deux formes graves de MPE, alors qu'ils ne le sont pas en cas de malnutrition modérée.
Dans le kwashiorkor, les protéines totales du sérum sont diminuées, surtout l'albumine. Cette réduction est moins marquée dans le marasme. Au contraire, les globulines sont souvent normales, voire élevées, en raison des infections. La diminution de l'albumine n'apparaît que dans un kwashiorkor cliniquement évident. Le taux d'albumine ne permet pas de prédire l'évolution d'une malnutrition modérée vers un kwashiorkor, alors que, dans un kwashiorkor avéré, sa diminution est proportionnelle à la gravité.
On admet généralement qu'un taux d'albumine inférieur à 3 g/dl est bas, et qu'en dessous de 2,5 g/dl le déficit est sérieux (voir tableau 22). On estime aussi que 2,8 g est le seuil d'alerte indiquant une évolution imminente vers une MPE grave.
Le taux d'albumine sérique est un examen facile et peu onéreux qui, contrairement aux examens ci-dessous, peut être fait dans des laboratoires modestes.
Les taux de deux autres protéines sériques, la préalbumine et la transferrine, sont également utiles et pas trop difficiles à mesurer. Elles diminuent toutes deux dans le kwashiorkor et peuvent aider à en estimer la gravité. Mais le taux de transferrine est lié au statut du fer, ce qui réduit son intérêt comme indicateur de kwashiorkor.
Le taux de la protéine porteuse du rétinol est également diminué dans le kwashiorkor et, à un degré moindre, dans le marasme. Mais il peut aussi être influencé par des affections hépatiques, un déficit en vitamine A ou en zinc et une hyperthyroïdie.
D'autres examens utilisés ou recommandés dans le diagnostic et l'évaluation de la MPE ont un intérêt limité, notamment:
Aucun de ces tests n'est spécifique et la plupart ne sont pas réalisables dans le laboratoire d'un hôpital de district.
TABLEAU 22
Taux d'albumine sérique chez les enfants
mal nourris
Taux (g/dl) |
Signification |
> ou = 3,5 |
Normal |
3-3,4 |
Subnormal |
2,5-2,9 |
Bas |
< ou = 2,5 |
Pathologique |
Source: Alleyne et al., 1977.
Tous les enfants atteints de kwashiorkor grave, de marasme ou de kwashiorkor marastique devraient être hospitalisés avec leur mère. L'enfant devrait être examiné avec soin, notamment pour rechercher une infection, pulmonaire en particulier, pneumonie ou tuberculose, puis pesé et mesuré. Il faudrait ensuite pratiquer des examens des selles, d'urine et de sang (dosage de l'hémoglobine et recherche de paludisme).
Il arrive que l'enfant ne puisse pas être traité à l'hôpital; dans ce cas, il faut le traiter au mieux dans le dispensaire le plus proche. Si l'enfant est encore allaité, il faut évidemment poursuivre l'allaitement.
Alimentation. Le traitement repose souvent sur le lait écrémé en poudre1 qui peut être reconstitué sur place en ajoutant une cuillère à café de poudre de lait à 25 ml d'eau bouillie et en mélangeant soigneusement. Il faut donner à l'enfant 150 ml de ce mélange par kg de poids corporel et par jour, répartis en six repas, toutes les quatre heures environ. Un enfant de 5 kg doit donc recevoir 5 x 150 = 750 ml par jour divisés en six repas, soit 125 ml par repas, obtenu en ajoutant cinq cuillères à café de poudre à 125 ml d'eau.
Il faut donner le lait à l'enfant à l'aide d'une tasse et d'une cuillère. Si cela s'avère difficile parce que l'enfant n'a pas beaucoup d'appétit ou parce qu'il est gravement malade, la meilleure solution consiste à utiliser une sonde nasogastrique: en polyéthylène de 50 cm de long et de 1 mm de diamètre intérieur. La sonde passe par une narine, et il faut fixer l'extrémité sur la joue avec du sparadrap ou un pansement à l'oxyde de zinc. On peut la laisser en place sans problèmes pendant cinq jours. L'idéal est de faire passer le lait en continu, comme s'il s'agissait d'une perfusion. Sinon, on peut pousser le lait à l'aide d'une seringue à intervalles réguliers environ toutes les quatre heures. Avant et après chaque repas, il faut injecter 5 ml d'eau tiède bouillie pour éviter l'obstruction de la sonde.
Il existe des mélanges plus élaborés que le lait écrémé en poudre ordinaire, que l'on peut administrer de la même manière à la cuillère ou par sonde gastrique. La plupart de ces mélanges contiennent une huile végétale (sésame, graines de coton), de la caséine (protéine du lait purifiée), du sucre et du lait en poudre écrémé. L'huile augmente l'apport calorique et la densité du mélange, tout en étant mieux tolérée que les graisses du lait entier. L'adjonction de caséine accroît le coût mais réduit souvent la durée d'hospitalisation, ce qui la justifie. Il existe une formule de ce mélange baptisé "SCOM" (Sugar, Casein, Oil, Milk, c'est-à-dire sucre, caséine, huile, lait) qui est facile à mémoriser: une dose de sucre, une dose de caséine, une dose d'huile, une dose de lait écrémé en poudre auxquelles on ajoute de l'eau pour obtenir 20 doses. Le mélange sec peut être stocké un mois dans une boîte métallique hermétique. Il suffit, pour préparer un repas, de prélever la quantité de poudre nécessaire dans un récipient et d'ajouter l'eau, et de remuer, ou mieux fouetter, le mélange pour le rendre homogène. Comme pour le lait écrémé en poudre ordinaire, il faut en administrer 150 ml/kg/jour, soit pour un enfant de 5 kg, six repas de 125 ml obtenus en mélangeant quatre cuillères à café du mélange sec à 125 ml d'eau; 30 ml de ce mélange procurent 28 kcal, 1 g de protéines et 12 mg de potassium.
Réhydratation. Les enfants qui ont une diarrhée grave et/ou accompagnée de vomissements sont souvent déshydratés. Une perfusion intraveineuse n'est nécessaire que si les vomissements sont incoercibles ou si l'enfant refuse de boire. L'utilisation d'une solution de réhydratation orale (SRO) standard suffit comme dans toute diarrhée (voir chapitre 37). Pour les enfants gravement mal nourris, il peut être avantageux de diluer davantage la SRO, en mélangeant par exemple à 1,5 litre d'eau bouillie un sachet prévu pour 1 litre.
Hypothermie. Même dans les pays tropicaux, la température nocturne diminue souvent considérablement, que ce soit dans les hôpitaux ou ailleurs. Un enfant mal nourri a du mal à maintenir sa température et peut laisser celle-ci chuter. En l'absence de traitement, l'hypothermie est une des causes de décès de ces enfants. Alors qu'à la maison l'enfant dort avec sa mère qui le réchauffe, à l'hôpital, il est seul et parfois exposé à des courants d'air. Dès que la température descend au-dessous de 36ºC, il faut réchauffer l'enfant: l'habiller chaudement, le couvrir et maintenir la pièce la plus chaude possible. On peut aussi utiliser des bouillottes remplies d'eau chaude. Il faut vérifier fréquemment la température.
Médicaments. Bien qu'il soit utile d'établir des protocoles de traitement des malnutritions graves dans les hôpitaux, chaque enfant doit néanmoins faire l'objet d'un traitement personnalisé et adapté à ses besoins.
Les infections sont si courantes chez les mal nourris que les antibiotiques sont souvent prescrits de façon systématique. On utilise souvent la benzyl-pénicilline IM à raison d'un million d'unités par jour réparties en plusieurs prises pendant cinq jours; ou l'ampicilline à raison de 4 comprimés à 250 mg par jour; ou l'amoxicilline à raison de 3 comprimés à 125 mg par jour. On a moins souvent recours à la gentamycine ou au chloramphénicol.
Dans les zones d'endémie palustre, il est souhaitable d'administrer un demi comprimé de chloroquine (125 mg) par jour pendant trois jours, puis une fois par semaine. Dans les cas graves et en cas de vomissements, il faut utiliser la chloroquine injectable.
En cas d'anémie grave, il convient de transfuser puis d'administrer du sulfate de fer trois fois par jour.
Si l'examen des selles met en évidence des ankylostomes, des ascaris ou d'autres parasites, il faut donner de l'albendazole ou un produit similaire une fois que l'état de l'enfant s'est un peu amélioré.
Etant donné la fréquence de la tuberculose chez les enfants mal nourris, il faut systématiquement la rechercher et administrer le traitement adapté, le cas échéant.
Avec le traitement ci-dessus, un enfant atteint de kwashiorkor grave doit commencer à perdre ses œdèmes entre le troisième et le septième jour, et donc perdre du poids. Parallèlement, la diarrhée se calme ou disparaît, les lésions cutanées commencent à s'estomper et l'enfant retrouve un peu de sa vivacité.
Quand la diarrhée a disparu, que les œdèmes ont fondu et que l'appétit est revenu, il faut arrêter la sonde gastrique si c'est la méthode qui a été utilisée. On peut poursuivre l'alimentation à base de SCOM ou de lait écrémé en poudre ordinaire à la tasse et à la cuillère, en aucun cas au biberon. En cas d'anémie, il faut commencer un traitement par fer oral et donner un demi comprimé de chloroquine par semaine.
Les enfants présentant un marasme grave consomment souvent des quantités de calories impressionnantes et leur prise de poids est rapide. Par contre, la durée totale du traitement et la durée de l'hospitalisation sont souvent plus longues que pour le kwashiorkor.
Dans les deux cas, la prise de poids débute en général au cours de la deuxième semaine. Tout en continuant l'administration de lait, il faut introduire progressivement une alimentation variée afin de fournir les calories, les protéines, les minéraux et les vitamines nécessaires.
Pour éviter les rechutes, il est nécessaire de faire participer la mère ou la personne qui s'occupe de l'enfant aux repas. Il faut lui expliquer ce que l'on donne et pourquoi. Pour assurer sa coopération dans l'immédiat et la mise en œuvre des recommandations à la maison à l'avenir, il faut utiliser à l'hôpital des ingrédients disponibles à domicile, ou au moins disponibles dans la région. Dans une région où le maïs est l'aliment de base, on peut donner à l'enfant une bouillie de maïs en ajoutant du lait écrémé en poudre. Pour un enfant plus âgé, on peut ajouter deux fois par jour des arachides écrasées à sa bouillie ou lui donner des arachides grillées. On peut donner aussi quelques cuillères de fruits mûrs (papaye, mangue, orange, etc.). Lors des deux repas principaux, la mère peut ajouter une petite portion des légumes verts, des légumineuses, du poisson ou de la viande qu'elle prépare pour le reste de la famille en prenant soin de bien les écraser. On peut donner des aliments riches en protéines comme des légumineuses, des arachides, de la viande, du lait fermenté ou des œufs. Si les œufs sont disponibles et culturellement acceptables, on peut les donner brouillés, durs ou mélangés crus à une bouillie et montrer à la mère comment les préparer. Les protéines animales sont souvent trop chères, mais elles peuvent être remplacées par un mélange de céréales et de légumineuses. Si les aliments riches en vitamines sont rares, il convient d'administrer un supplément vitaminique car ni le lait écrémé en poudre ni le SCOM ne sont riches en vitamines.
Tout comme le maïs cité plus haut, l'alimentation peut aussi bien être basée sur du riz ou du blé. Si l'aliment de base est le manioc ou la banane plantain, pauvres en protéines, il faut s'assurer d'un bon apport protéique par ailleurs.
Après la sortie de l'hôpital ou le traitement à domicile s'il s'agit d'un cas bénin, il faut suivre l'enfant en consultation, de préférence en dehors de la foule bruyante des consultations générales, soit l'après-midi soit dans une consultation de protection maternelle et infantile. La personne qui reçoit la mère doit travailler au calme et avoir assez de temps pour lui expliquer ce qu'on attend d'elle et vérifier que les recommandations ont été comprises. Il est inopérant de se contenter de tendre à la mère un sachet de lait en poudre ou d'un supplément quelconque ou encore de se contenter de peser l'enfant sans donner de conseils.
Une prise de poids satisfaisante est un bon indicateur de progrès. Il faut donc peser l'enfant à chaque visite et noter le poids sur une courbe de façon à le visualiser autant pour l'agent de santé que pour la mère.
Le suivi repose sur la fourniture d'un supplément nutritionnel adapté, mais il est préférable de l'intégrer aux repas. Il faut donner à la mère une cuillère-doseur et lui expliquer combien elle doit en ajouter aux autres aliments chaque jour selon le poids de l'enfant. Il est préférable de mélanger les suppléments, notamment le lait écrémé en poudre, aux aliments de l'enfant (à une bouillie de céréales par exemple) plutôt que de faire une préparation séparée. Il faut s'enquérir du nombre de repas offerts à l'enfant: s'il n'est nourri que deux fois comme le reste de la famille, il faut demander à la mère de lui donner deux repas de plus.
Lorsque cela est possible, une bonne solution consiste à donner le SCOM en consultation externe sous forme de mélange sec, prêt à l'emploi en sacs de polyéthylène fermés.
La majorité des décès d'enfants gravement mal nourris survient dans les trois premiers jours d'hospitalisation. Le taux de décès dépend de nombreux facteurs, notamment la gravité de la malnutrition, l'état de l'enfant et la qualité du traitement. Dans certaines sociétés, les enfants sont amenés à l'hôpital très tard, alors qu'ils sont mourants, et le taux de décès est alors très élevé.
Le pronostic dépend de la cause et de la gravité de la maladie. Chez un enfant atteint de marasme grave avec des poumons très endommagés par une tuberculose, le pronostic est évidemment médiocre. Le pronostic d'un marasme modéré sans infection est bien meilleur. La réponse au traitement est meilleure pour les kwashiorkors que pour les marasmes.
Il est souvent difficile de savoir quoi faire quand l'enfant est guéri, surtout s'il a moins de 1 an. Parfois l'enfant a perdu sa mère ou elle est malade ou elle n'a pas assez de lait. Il est vital d'apprendre à la personne qui va s'occuper de l'enfant comment le nourrir correctement. Si c'est le père qui a amené l'enfant, il faut demander à une femme de la famille de passer quelques jours à l'hôpital avant la sortie de l'enfant. Il faut lui apprendre à nourrir l'enfant avec une tasse et une cuillère et à ne jamais utiliser de biberon sauf si l'enfant a moins de 3 mois. Le meilleur système consiste à préparer une bouillie peu épaisse à partir de l'aliment de base local auquel on ajoute deux cuillères à café de lait écrémé en poudre (ou d'un autre supplément riche en protéines) et deux cuillères d'huile par kg de poids et par jour. Si l'enfant a plus de 6 mois, il faut également expliquer quels autres aliments ajouter. Il faut demander à la mère ou à son substitut de revenir en consultation une fois par semaine si elle n'habite pas trop loin (dans un rayon de 10 km) ou une fois par mois dans le cas contraire. Il faut lui remettre des suppléments pour une durée légèrement plus longue que l'intervalle prévu entre deux consultations. Pour les autres aliments adaptés à l'enfant, on trouvera des détails au chapitre 6.
L'alimentation doit absolument apporter suffisamment d'énergie et de protéines. On compte généralement 120 kcal et 3 g de protéines par kg et par jour. Un enfant de 10 kg doit donc recevoir 1 200 kcal et 30 g de protéines chaque jour. Cependant, un enfant atteint de marasme est capable de consommer et d'utiliser 150 à 200 kcal et 4 à 5 g de protéines par kg et par jour.
On sait maintenant que la MPE touche les adultes, surtout dans les communautés qui manquent chroniquement de protéines. Ces patients sont très maigres pour leur taille sauf s'ils ont des œdèmes majeurs, leurs muscles ont fondu et leur graisse sous-cutanée a disparu. Les troubles du comportement sont fréquents: le malade a l'air de se désintéresser de son sort et de vivre hors de la réalité. Il est difficile d'attirer son attention et plus encore de la fixer. L'appétit est médiocre et le patient est faible.
Il y a presque toujours des œdèmes à un degré variable qui peuvent parfois masquer l'amaigrissement. Les œdèmes peuvent affecter l'ensemble du corps, mais ils prédominent au niveau des jambes et du scrotum. Le visage est souvent gonflé. On les appelle "œdèmes de famine" et on a rapporté de nombreux cas en Indonésie et en Papouasie-Nouvelle-Guinée.
Les selles sont fréquentes, molles et nauséabondes. L'abdomen est souvent distendu mais on peut aisément palper les organes tant la paroi est mince. La palpation induit des gargouillis et des mouvements péristaltiques. Les patients considèrent souvent leur maladie comme la conséquence d'une gastro-entérite et recourent fréquemment, avant d'aller à l'hôpital, à des purgatifs, pharmaceutiques ou fabriqués à partir de plantes locales, ou encore à des lavements à base de poivre, ce qui aggrave évidemment leur état.
Les cheveux sont abîmés et la peau est sèche et squameuse, ressemblant à un dallage irrégulier, surtout en regard des tibias. Les parotides sont souvent gonflées, fermes et caoutchouteuses à la palpation.
Il y a presque toujours une anémie souvent grave. La tension artérielle est faible. Il n'y a que des traces d'albumine dans les urines.
L'anémie peut se confondre avec une MPE car elle provoque des œdèmes, mais aussi une dyspnée et une cardiomégalie habituellement absentes dans la MPE, et elle ne s'accompagne pas d'altérations des cheveux et de la peau ou des parotides. Cependant, les deux maladies sont étroitement liées et souvent concomitantes.
Contrairement au kwashiorkor qui est rare, le marasme est très fréquent et résulte de cinq causes principales.
Apport alimentaire insuffisant. Tout enfant ou adulte dont l'apport alimentaire est très pauvre en calories aura des signes de marasme pouvant aboutir au décès. Les famines sont dues soit à des guerres extérieures ou intérieures, soit à des catastrophes naturelles comme la sécheresse, les inondations ou les tremblements de terre et provoquent les mêmes symptômes de marasme chez les adultes que chez les enfants: amaigrissement, diarrhée, infections, etc.
Infections. Ce sont surtout les infections chroniques non traitées ou incurables. Actuellement, il s'agit surtout du sida dû au virus VIH qui provoque un amaigrissement majeur à mesure que la maladie progresse. C'est de là que vient le nom de "slim disease" ("maladie de la maigreur") qu'on lui a attribué en Ouganda depuis longtemps (voir chapitre 3). La tuberculose à un stade avancé et d'autres infections aboutissent au même tableau.
Malabsorption. L'incapacité génétique ou acquise de l'appareil digestif à digérer ou absorber certains aliments aboutit également à un marasme en l'absence de traitement: mucoviscidose, maladie c_liaque, sprue, etc.
Cancers. A un stade avancé, tous les cancers entraînent une cachexie chez tous les patients.
Troubles du comportement alimentaire. L'anorexie mentale qui touche surtout les adolescentes dans les pays riches ainsi que d'autres perturbations psychologiques peuvent aboutir à une MPE.
Le traitement doit à la fois combattre la cause de la MPE, si c'est possible, et renutrir le patient. On peut traiter une tuberculose ou une amibiase, mais pas un cancer avancé ou un sida. La renutrition repose sur les mêmes principes que chez l'enfant. Les procédures de nutrition en situation d'urgence et de réhabilitation des victimes de famine décrites au chapitre 24 s'appliquent à la MPE de l'adulte.
La prévention de la MPE en Asie, en Afrique et dans les Amériques constitue un défi majeur, bien plus ardu que la lutte contre des carences isolées en iode ou en vitamine A, parce que ses causes sont multiples et complexes, et surtout parce qu'il n'existe pas une stratégie unique, universelle, peu coûteuse et pérennisable qui permette d'en réduire la prévalence ou la gravité.
La cinquième partie de ce manuel comporte diverses stratégies destinées à réduire la prévalence de la MPE. Elle suggère des politiques et des programmes nutritionnels adaptés, et différents chapitres sont consacrés à la sécurité alimentaire, à la protection de la santé et aux pratiques assurant une alimentation correcte. Ces chapitres offrent des conseils pour faire face aux trois causes principales de la MPE, c'est-à-dire le manque de nourriture, de soins et les maladies, inclus dans le cadre conceptuel du chapitre 1. D'autres chapitres discutent des solutions à certains aspects particuliers du problème, comme l'amélioration de la qualité et de la sécurité des aliments, la promotion d'une alimentation et d'un style de vie sains, la disponibilité alimentaire et la manière d'incorporer les objectifs nutritionnels aux politiques et programmes de développement. Toute cette partie met l'accent sur l'amélioration de la qualité de vie des populations par le biais de la lutte contre la pauvreté, l'amélioration de l'alimentation et la promotion de la santé, ainsi que sur la nécessité d'augmenter l'apport énergétique des personnes à risque de MPE.
A la fin des années 50 et 60, on estimait que la MPE était due surtout à un manque de protéines, et la solution semblait être le recours à des aliments riches en protéines. Cette stratégie malencontreuse a détourné l'attention du premier besoin, qui était celui d'un apport alimentaire suffisant aux enfants. Actuellement, on met beaucoup moins l'accent sur les aliments de sevrage riches en protéines et sur les efforts éducatifs visant à augmenter la consommation de viande, de poisson ou d'œufs qui sont inabordables pour la majorité des familles dont les enfants souffrent de MPE.
Bien que les protéines soient essentielles, la MPE est plus souvent liée à un apport alimentaire insuffisant qu'à un défaut de protéines. Quand une alimentation à base de céréales locales répond aux besoins caloriques, elle répond généralement aussi aux besoins protéiques, surtout si elle est accompagnée d'une petite quantité de légumineuses. Il faut donc s'attacher en premier lieu à assurer un apport suffisant et à réduire les infections.
Il faut s'efforcer de promouvoir et de protéger l'allaitement maternel et les bonnes pratiques de sevrage, d'augmenter la consommation par les jeunes enfants de céréales, de légumineuses et autres aliments de sevrage locaux; de prévenir et de contrôler les infections bactériennes ou parasitaires; d'augmenter la fréquence des repas des jeunes enfants; et, si cela s'avère approprié, d'encourager une plus grande consommation d'huiles et de graisses diverses qui augmentent l'apport calorique sans accroître le volume des repas. L'impact de ces mesures sera d'autant plus marqué qu'elles s'accompagneront d'une surveillance de la croissance, de vaccinations, de thérapie de réhydratation orale pour les diarrhées, de traitement précoce des maladies courantes, de déparasitages réguliers et d'attention aux causes sous-jacentes de MPE que sont la pauvreté et l'inégalité. Certaines de ces mesures peuvent être mises en œuvre dans le cadre des soins de santé primaires. Tous les lecteurs qui s'intéressent à la prévention de la MPE trouveront plus de détails dans la cinquième partie de ce manuel.
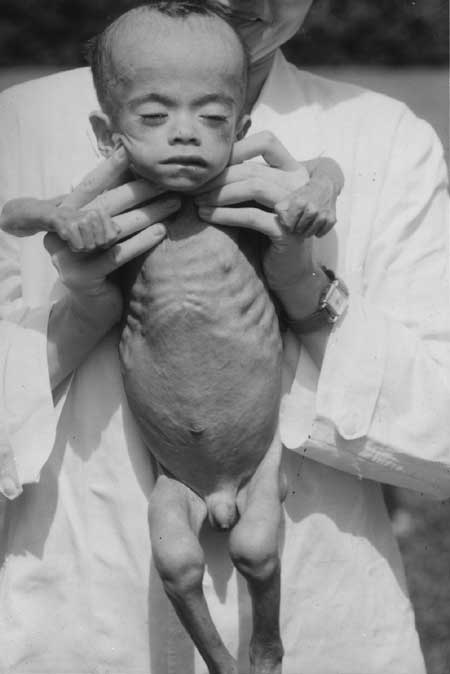
PHOTO 15
Marasme avec amaigrissement extrême à Rotterdam (Pays-Bas) pendant la seconde guerre mondiale
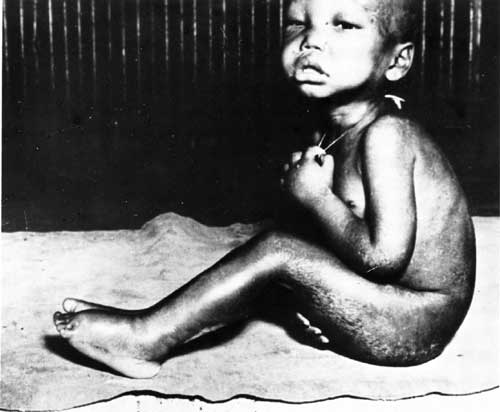
PHOTO 16
Dermatose caractéristique des cuisses, des bras et du dos et œdèmes des jambes et du visage masquant la fonte musculaire chez un enfant atteint de kwashiorkor
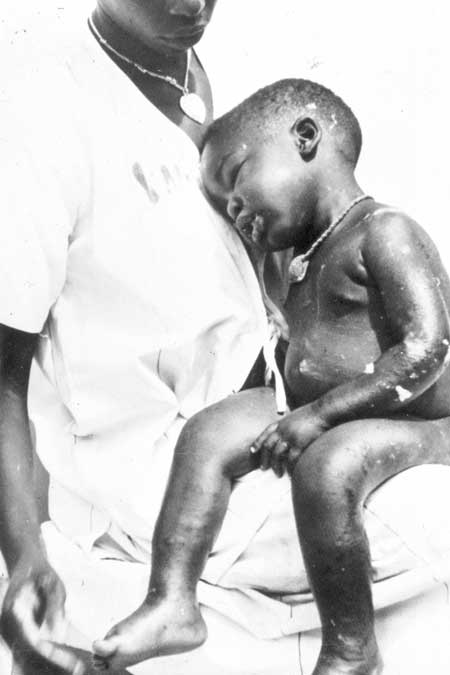
PHOTO 17
œdèmes, altérations cutanées et ulcération du coude chez un enfant atteint de kwashiorkor

PHOTO 18
Marasme chez un enfant colombien
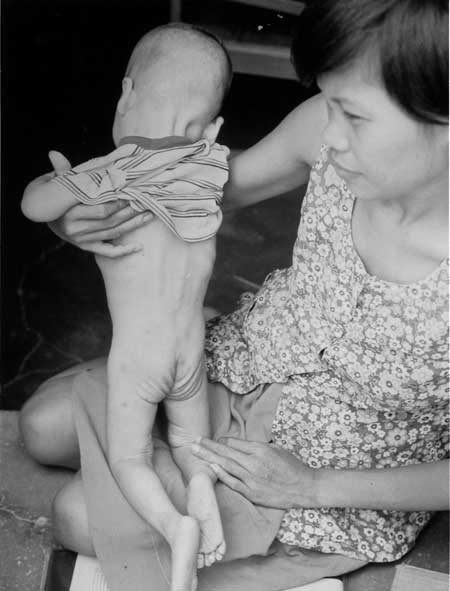
PHOTO 19
Disparition manifeste de la graisse sous-cutanée chez un enfant philippin atteint de marasme
1 Il faut s'assurer que l'enfant reçoit tous les micronutriments dont il a besoin. Il est déconseillé d'utiliser du lait écrémé en poudre non vitaminé.