Влияние изменения климата на вредные для растений организмы
Анализ конкретных примеров по отдельным видам вредных организмов
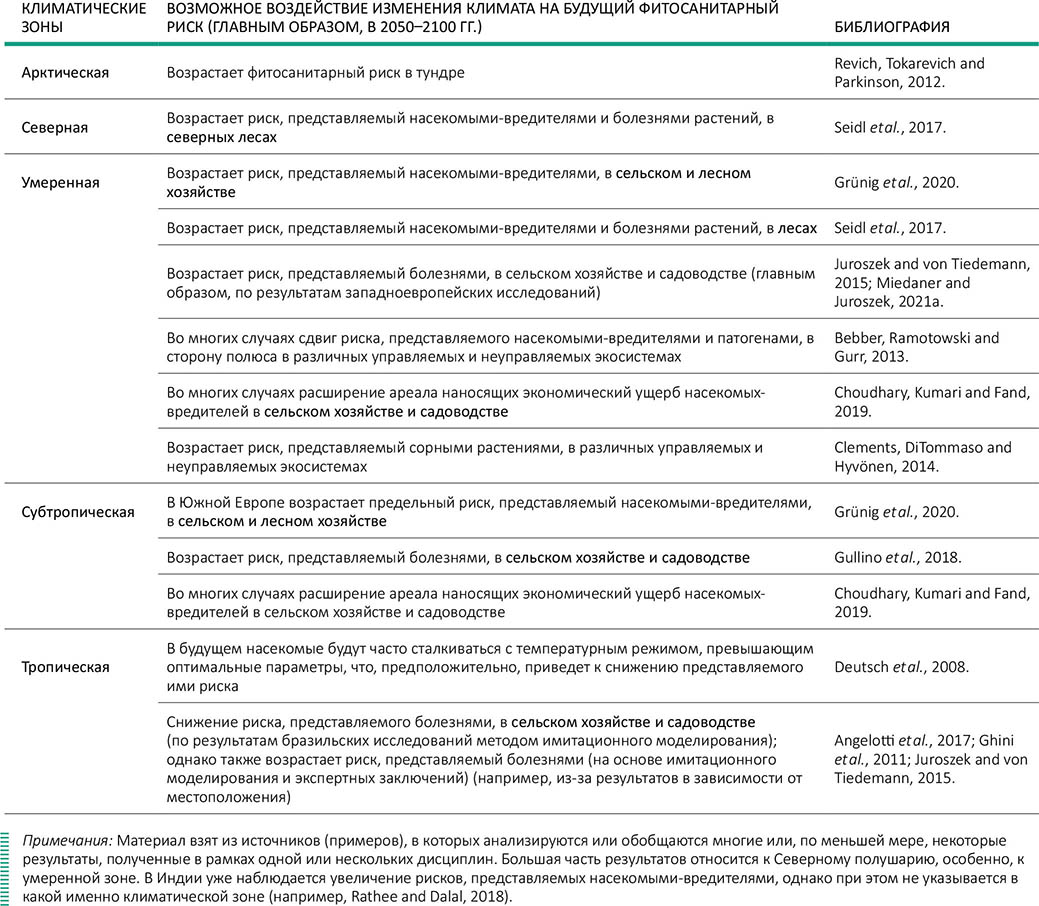
Некоторые вредные организмы уже расширили спектр своих хозяев или распространенность, по крайней мере отчасти, вследствие изменения климата. Ниже описываются примеры таких вредных организмов, выбранных в зависимости от их вредоносности в различных географических зонах. Примеры некоторых возможных последствий воздействия изменения климата на вредные для растений организмы (насекомых, патогены и сорные растения) в различных климатических зонах приведены в таблице 3.
Таблица 3 Примеры некоторых возможных последствий воздействия изменения климата на вредные для растений организмы (насекомых, патогены и сорные растения) в разных климатических зонах
Насекомые
1. Ясеневая изумрудная златка (Agrilus planipennis) (Азия, Европа, Северная Америка)
Ясеневая изумрудная златка Agrilus planipennis – жук-лубоед, заселяющий ясени (Fraxinus spp.) (EPPO, 2021b). Взрослые особи питаются листьями ясеня, однако именно из-за того, что личинки экстенсивно питаются флоэмой и камбрием, нарушается передвижение веществ в дереве, дереву наносятся кольцевые повреждения (т.е. повреждение кольца коры по всей окружности ветки или ствола), и, в конечном итоге, оно погибает.
Родом из северо-восточной части Китая, с Корейского полуострова и востока Российской Федерации, ясеневая изумрудная златка распространилась в другие части Азии, Северную Америку (Канаду и Соединенные Штаты Америки) (Haack et al., 2002) и в Европу (в частности, в западную и южную части Российской Федерации и Украину) (CABI, 2021b). Например, этот вредитель, вероятно, был интродуцирован в Северную Америку в 2002 году с древесными упаковочными материалами. Дендрологические исследования показывают, что он прибыл на континент приблизительно за десятилетие до своего обнаружения. Последующему распространению этого жука в различные части Соединенных Штатов Америки и Канады, вероятно, способствовало перемещение зараженных сеянцев, бревен и топливной древесины (Herms and McCullough, 2014; Ramsfield et al., 2016).
Этот вредитель оказывает разрушительное воздействие. По мнению Aukema et al. (2011), это самое вредоносное и дорогостоящее инвазивное лесное насекомое в Соединенных Штатах Америки, экономические потери из-за которого, по прогнозам, к 2020 году превысят 12,5 млрд. долларов США. Нашествие этого жука также серьезно отразилось на биоразнообразии в зараженных зонах, поскольку ясени служат источником пищи, укрытием и средой обитания для многих видов. Более того, нашествие ясеневой изумрудной златки и последующая потеря деревьев позволяет говорить о возможных последствиях для здоровья человека (Donovan et al., 2013). Стратегии борьбы направлены на локализацию, например, посредством использования карантинных зон, и на сокращение плотности популяций, в частности, путем интродукции агентов биологической борьбы. Изначально предпринимались попытки ликвидации, но позднее от нее отказались (Herms and McCullough, 2014).
Распространенность ясеневой изумрудной златки, в основном, ограничивается местами произрастания ясеня, тем не менее, считается, что климат также играет важную роль. В своем родном ареале ясеневая изумрудная златка живет только в части ареала произрастания ясеня, однако моделирование, описанное в работе Liang and Fei (2014), показывает, что изменение климата приведет к распространению этого жука в более северных районах Северной Америки и последующему долговременному риску для ясеня в этих районах. Однако ожидается, что продвижение ясеневой изумрудной златки на юг Северной Америки будет ограничено рамками условий потепления климата, поскольку этому жуку требуются ярко выраженные сезонные изменения с долгим зимним периодом. Описанное в работе Duan et al. (2020) исследование зимней выживаемости личинок нескольких интродуцированных видов паразитоидов ясеневой изумрудной златки после экстремального климатического явления (низких зимних температур) также показало, что экстремальные климатические явления, связанные с изменением климата, могут снизить эффективность биологической борьбы с этим жуком.
2. Мухи-пестрокрылки (во всем мире)
Мухи-пестрокрылки – это семейство разнообразных насекомых, в которое входит более 4 тыс. описанных видов. Большая часть видов питается растениями, а некоторые могут наносить существенный экономический ущерб, особенно в случае, когда их личинки развиваются в плодах, имеющих высокую рыночную ценность. В семейство входит несколько инвазивных видов, например, Bactrocera oleae (Gutierrez et al. 2009), к кормовой базе этого вида относятся только оливковые деревья (и некоторые дикорастущие родственники), Bactrocera dorsalis, поражающая несколько десятков видов плодовых растений, и средиземноморская муха Ceratitis capitata, повреждающая некоторое число древесных культур.
Мухи-пестрокрылки смогли распространиться на новые территории из своего первичного ареала и заселили как соседние районы, так и новые регионы, благодаря расширению зон выращивания их растений-хозяев, международной торговле, а также благодаря тому, что изменение климата позволило им выживать зимой и размножаться в средах обитания, которые иначе были бы для этих видов непригодны. Bactrocera oleae присутствует в Африке, Европе и Азии, а также недавно распространилась в Калифорнии и Мексике (CABI, 2021c). Однако в работе Godefroid et al. (2015) был сделан вывод, что этот вид может акклиматизироваться не только в средиземноморских регионах с умеренным климатом, но и в более прохладном климате северных широт Европы, где оливковые деревья еще предстоит выращивать.
Bactrocera dorsalis – вредитель, вызывающий серьезное беспокойство на всей территории юго-восточной Азии и западнее до Пакистана, а также с севера до юга Китая и Непала. Сообщается о его обнаружении в других зонах, в том числе на большей части территории Африки, на востоке Соединенных Штатов Америки и на нескольких островах Тихого океана (EPPO, 2021c). Поскольку у этой мухи более широкий спектр растений-хозяев, ее часто выявляют на международных рынках. Так как B. dorsalis может обитать, главным образом, в тропиках и субтропиках, и считается, что требования для ее выживания – довольно сложные, то риск непосредственного экономического ущерба в случае возникновения первичного очага в зонах с умеренным климатом – низкий, однако изменение климата вследствие глобального потепления может способствовать стремительному увеличению популяций этой мухи в мягком климате с учетом того, что зимовать она будет в защищенных условиях в плодах, которые хранятся в закрытых местах (EPPO, 2021c). Также это относится и к C. capitata, распространенной на юге и в центре Европы, на большей части территории Африки и на Ближнем Востоке, в Центральной и Южной Америке, а также в Западной Австралии, однако ее личинки также могут зимовать в более холодных регионах в плодах, которые хранятся в теплом месте. Она может распространяться в процессе международной торговли апельсинами, мандаринами и лимонами (Fedchock et al., 2006).
3. Красный пальмовый долгоносик (Rhynchophorus ferrugineus) (Ближний Восток, Африка, Европа)
Красный пальмовый долгоносик Rhynchophorus ferrugineus относится к насекомым-вредителям пальм, наносящим наибольший экономический ущерб. Его родина – юго-восточная часть Азии и Меланезия. Личинки этого долгоносика питаются внутри конуса нарастания дерева, существенно повреждая ткань растения, ослабляя его структуру и во многих случаях приводя к гибели. В странах Персидского залива на Ближнем Востоке ежегодные потери вследствие гибели и уничтожения пальм, сильно зараженных красным пальмовым долгоносиком, оцениваются от 5,2 млн. до 25,9 млн. долларов США при уровне заражения 1 и 2 процента, соответственно (El-Sabea, Faleiro and Abo-El-Saad, 2009). По другим оценкам ежегодные потери из-за красного пальмового долгоносика составляют 15 млн. долларов США (Al-Ayedh, 2017).
Красный пальмовый долгоносик наносит вред разным видам пальм, в том числе кокосовой и финиковой пальмам (El-Mergawy and Al-Ajlan, 2011; FAO, 2020). Впервые заражение финиковых пальм на Ближнем Востоке было обнаружено в середине 1980-х, и впоследствии этот вредитель распространился по территории других стран Ближнего Востока, Африки и Европы. В 2010 году его выявили в Калифорнии в Соединенных Штатах Америки, и в 2015 году было объявлено о его ликвидации. Его распространению по всему миру, вероятно, способствовало перемещение отводков пальмы в качестве посадочного материала. Стратегии борьбы заключаются в использовании различных агротехнических и фитосанитарных мер, таких как уничтожение зараженных деревьев, применение инсектицидов и энтомопатогенных нематод, а также использование феромонных ловушек (FAO, 2020; Ge et al., 2015).
Из-за изменения климата может расшириться распространенность красного пальмового долгоносика. В работе Ge et al. (2015) делается прогноз, что в Китае с изменением климата вырастет число крайне благоприятных для этого вредителя зон, что приведет к его распространению в северной части Китая. Красный пальмовый долгоносик – единственный вид семейства Rhynchophorus, значительно расширивший свой первоначальный ареал в Южной и Юго-Восточной Азии (Wattanapongsiri, 1966). Сообщается о его присутствии в 45 странах, а моделирование экологической ниши показывает, что этот вредитель будет и дальше расширять свой ареал (Fiaboe et al., 2012). Красный пальмовый долгоносик все еще считается серьезной проблемой растениеводов, занимающихся выращиванием пальм на Ближнем Востоке, и, несмотря на интегрированные меры борьбы, он все еще вызывает огромные экономические потери.
4. Кукурузная лиственная совка (Spodoptera frugiperda) (Северная и Южная Америка, Африка, Азия)
Кукурузная лиственная совка (Spodoptera frugiperda) – это совка, относящаяся к семейству Noctuidae (рис. 7). Спектр ее растений-хозяев исчисляется сотнями видов растений, она наносит серьезный ущерб травам, особенно кукурузе и сорго, которым она отдает предпочтение, а также другим сельскохозяйственным культурам, в частности, рису, хлопку и сое, которые предпочитают разные расы этого вида. Ее родина – тропические и субтропические зоны Северной и Южной Америки, а летом она мигрирует в южные и северные части американских континентов с умеренным климатом. Впервые этого вредителя обнаружили на западе Африки в 2016 году (Goergen et al. 2016), а затем в странах Африки к югу от Сахары и в Египте в 2019 году. В 2018 году сообщалось о присутствии кукурузной лиственной совки в Индии, она стремительно распространилась по всей южной и восточной части Азии, включая Китай, Республику Корея, Японию и Пакистан. Также сообщалось о ее присутствии в Бангладеш, Индонезии, Мьянме, Шри-Ланке, Таиланде, Филиппинах, Вьетнаме и Йемене (EPPO, 2020a). В 2020 году кукурузная лиственная совка была впервые обнаружена на посевах кукурузы в Иордании и Объединенных Арабских Эмиратах (IPPC Secretariat, 2020a; 2020b), а также в Израиле (EPPO, 2020b). Также она распространилась по территории Австралии (IPPC Secretariat, 2021).
Рисунок 7A

(а) Поврежденный гусеницами початок кукурузы; (б) гусеница и повреждение кукурузы на стадии выметывания.
Рисунок 7Б

Кукурузная лиственная совка приспособлена к теплому климату и не может входить в состояние диапаузы, ее географическая распространенность в значительной степени зависит от климатических условий. Взрослые особи могут преодолевать до нескольких километров за одну ночь, а во время сезонной миграции долетать до Канады из южной части Соединенных Штатов Америки. В работе Ramirez-Cabral, Kumar and Shabani (2017) отмечается расширение ее ареала в более теплом климате благодаря приспосабливаемости к различной среде, хорошей способности к распространению, широкому спектру потенциальных хозяев и активной международной торговле товарами, которые личинки или куколки совки могут поражать. Также прогнозируется сокращение популяции или даже частичное исчезновение этого вида в южной части Западного полушария вследствие того, что в середине и конце этого века ожидаются более теплые и сухие условия на севере этого субконтинента. В Европейском союзе в некоторых теплых районах Испании, Италии и Греции могли бы возникнуть подходящие климатические условия для акклиматизации этого вида, особенно популяций, обосновавшихся на севере Африки (Jeger et al., 2018).
5. Пустынная саранча (Schistocerca gregaria) (Африка, Западная и Южная Азия)
Пустынная саранча (Schistocerca gregaria), в основном, присутствует в Африке, на территории Аравии и Западной Азии, в отдельных частях Южной Азии (FAO, 2021a). Сообщается о ее периодическом обнаружении на юго-западе Европы. Она роится и неистово уничтожает такие ключевые сельскохозяйственные культуры, как кукуруза и сорго, пастбища и всю зеленую растительность, которая встречается на ее пути, тем самым нанося значительный ущерб мелким фермерам и скотоводам (Kimathi et al., 2020).
Пустынная саранча демонстрирует периодическое изменение формы тела и от поколения к поколению может меняться в ответ на условия окружающей среды, превращаясь из обособленных, высоко плодовитых, немигрирующих насекомых в скопление мигрирующих особей, которые могут перемещаться на большие расстояния, в конечном итоге вторгаясь на новые территории. Как правило, пустынная саранча активно размножается в полузасушливых зонах, занимая территории с запада Африки через Ближний Восток до юго-запада Азии и представляя угрозу для обеспечения людей средствами к существованию в более чем 65 странах. Однако существует гораздо менее известный подвид – S. gregaria flaviventris, который обитает на ограниченной территории в южной части Африки, и необходимо изучить потенциал этого подвида представлять угрозу в будущем (Meynard et al., 2017).
В течение многих веков регистрировались крупные очаги пустынной саранчи, и ФАО ведет базу данных по многолетнему, крупномасштабному мониторингу в зараженных зонах. Важно определять потенциальные места размножения этого вредителя, если планируется принимать малозатратные и своевременные профилактические меры до того, как этот вредитель нанесет значительный ущерб (Kimathi et al., 2020). С 1960-х годов очаги возникали реже, однако в 2019-2020 гг. беспрецедентное размножение наблюдалось в Эритрее, Сомали и Йемене по причине необычайно сильных ливней в регионе Африканского Рога. Применяемая в настоящее время стратегия борьбы с роями саранчи заключается в аэроопрыскивании химическими пестицидами, что оказывает крайне неблагоприятное воздействие на людей, сельскохозяйственных животных, окружающую среду и биоразнообразие.
Поведение, экология и физиология пустынной саранчи меняется в ответ на некоторые климатические условия. Сложно объяснить отдельно взятое явление изменением климата, однако такие климатические изменения, как увеличение температуры и дожди в пустыне, а также сильные ветры, связанные с тропическими циклонами, создают новую благоприятную среду для размножения, развития и миграции этого вредителя. Это позволяет предположить, что глобальное потепление сыграло свою роль в создании условий, необходимых для развития, возникновения очагов и выживания саранчи. Однако влияние изменения климата имеет сложный характер, и поэтому Комиссия ФАО по борьбе с пустынной саранчой в Юго-Западной Азии (FAO, 2021a) отметила необходимость международного сотрудничества между зараженными странами в целях устранения угрозы, представляемой саранчой. Куда она полетит дальше, зависит от направления и скорости ветра, а также других погодных условий. Следовательно, изменение климата может повлиять на будущие пути миграции пустынной саранчи. Однако при прогнозировании риска в различных сценариях изменения климата, может потребоваться разграничение разных подвидов, поскольку они могут иметь разные требования к экологическим нишам.
Возбудители болезней растений
6. Ржавчина кофейного дерева (Hemileia vastatrix) (Африка, Азия, Латинская Америка)
Ржавчина кофейного дерева, вызываемая Hemileia vastatrix, является одним из основных факторов, ограничивающих урожайность кофе арабика по всему миру. Ранние и крайне агрессивные вспышки болезни за последние несколько лет привели к серьезным потерям (до 50-60 процентов урожая) в некоторых странах Латинской Америки, таких как Колумбия и Мексика.
По всей видимости, климат играет некоторую роль в распространении этой болезни. Одним из факторов, способствовавших возникновению эпидемии ржавчины в Центральной Америке, стало уменьшение суточной амплитуды температур, что сократило латентный период болезни (Avelino et al., 2015). Более короткий латентный период способствует быстрому увеличению популяции патогена. Аналогичным образом при глобальном потеплении может сократиться его инкубационный период. Анализ, проведенный в работе Ghini et al. (2011) в отношении будущих сценариев изменения климата в Бразилии, свидетельствует о тенденции сокращения инкубационного периода H. vastatrix, и это означает, что в течение одного вегетационного периода сможет развиться больше поколений этого патогена. Следовательно, в будущем может возрасти риск эпидемии ржавчины кофейного дерева при отсутствии прочих факторов, снижающих риск болезни, таких как снижение способности патогена к заражению кофейных деревьев. Менее холодные зимы могут привести к увеличению количества инокулята, упрощая заражение патогеном (Avelino et al., 2015), но холодные температуры могут не представлять проблемы для этого патогена, учитывая тот факт, что в Африке перенос производства кофе в более прохладные районы, расположенные выше над уровнем моря, не ограничил распространение ржавчины кофейных деревьев, поскольку этот патоген уже был широко распространен (Iscaro, 2014), и он может адаптироваться к разным климатическим условиям (Avelino et al., 2015). Таким образом, ржавчина кофейного дерева представляла и продолжает представлять одну из огромнейших проблем для мирового производства кофе, и потребуется выработка новых стратегий для обеспечения борьбы с ней, особенно в случае, если изменение климата повлияет на биологию этого патогена так, как указано в этих исследованиях.
7. Фузариозное увядание бананов (Fusarium oxysporum f. sp. cubense) тропической расы 4 (Австралия, Мозамбик, Колумбия, Азия, Ближний Восток)
Передающийся через почву гриб Fusarium oxysporum f. sp. cubense вызывает фузариозное увядание бананов. Выходом, найденным для борьбы с уничтожением бананов расой 1 патогена, стала посадка устойчивого культивара «кавендиш» (Ploetz, 2005; Stover, 1986). Однако новый штамм F. oxysporum – тропическая раса 4 (ТР4) – был обнаружен в 1990 году в Восточной Азии, некоторых частях Юго-Восточной Азии и в Северной Австралии. Он поражал клоны культивара «кавендиш» в тропиках (Ploetz, 2005; Ploetz and Pegg, 2000). С 2010 года эта раса распространилась в странах Южной и Юго-Восточной Азии (Вьетнам, Индия, Лаосская Народно-Демократическая Республика, Мьянма и Пакистан), на Ближнем Востоке (Израиль, Иордания, Ливан и Оман), в Африке (Мозамбик) (Dita et al., 2018) и Южной Америке (Колумбия) (Garcίa-Bastidas et al., 2019). Эта болезнь представляет огромную угрозу для производителей бананов «кавендиш» по всему миру, вне зависимости от того, являются они мелкими или крупными фермерами (Mostert et al., 2017). Высокие температуры, например, при повышении с 24 до 34 °C, и экстремальные погодные явления, включая циклоны и тропические штормы, могут увеличить риск болезни, особенно, когда растения бананов культивара «кавендиш» страдают из-за переувлажнения почвы (Pegg et al., 2019; Peng, Sivasithamparam and Turner, 1999). Поскольку до сих пор не существует культиваров банана, устойчивых к ТР4, и химическая борьба с патогеном не эффективна, единственный путь управления риском фузариозного увядания бананов (ТР4) – применение профилактических мер. Они включают, к примеру, использование свободного от болезни посадочного материала культивара «кавендиш», раннее выявление и уничтожение заболевших растений, как только замечаются симптомы фузариозного увядания (Pegg et al., 2019).
8. Xylella fastidiosa (Северная и Южная Америка, Южная Европа, Ближний Восток)
Xylella fastidiosa – грамотрицательная бактерия, поражающая ксилему. Она вызывает болезни экономически значимых культур, таких как виноград, цитрусовые, оливки, миндаль, персик и кофе, а также декоративных и лесных растений (Janse and Obradovic, 2010; Wells et al., 1987). Сообщалось о ее обнаружении в Северной и Южной Америке, а также в Азии, в 1980-х годах (Cornara et al., 2019). В 2013 году X. fastidiosa subsp. pauca поразила оливковые деревья на юге Италии, что привело к серьезным потерям и существенно изменило типичный местный ландшафт, поскольку этот патоген уничтожил столетние оливковые деревья (Saponari et al., 2013). X. fastidiosa переносится многочисленными видами сокососущих прыгающих насекомых, включая пенниц и цикадок, в основном, относящихся к семействам Aphrophoridae и Cicadellidae (Almeida et al., 2005; Cornara et al., 2019).
Модели биоклиматической распространенности видов показывают, что X. fastidiosa имеет потенциал расширить зону своей текущей распространенности и может распространиться в других районах Италии и в других странах Европы (Bosso et al. 2016; Godefroid et al., 2018). Идентифицированы разные подвиды этой бактерии: в основном, fastidiosa, multiplex и pauca. По прогнозам, полученным в результате моделирования, подвид multiplex и в некоторой степени подвид fastidiosa представляют угрозу для большей части территории Европы, тогда как зоны с подходящим для подвида pauca климатом, в основном, ограничены территорией средиземноморских стран (Godefroid et al., 2019). Прогностическая модель ранжирования рисков, примененная в недавнем исследовании Frem et al. (2020), показала, что бассейн Средиземного моря, особенно Ливан, подвергается наибольшему риску акклиматизации и распространения X. fastidiosa. Даже несмотря на то, что многие средиземноморские страны в настоящее время свободны от X. fastidiosa, в ближайшем будущем они будут подвержены высокому риску проникновения и акклиматизации X. fastidiosa: Турция больше всего подвержена риску, затем следуют Греция, Марокко и Тунис, для которых степень риска классифицируется как высокая. Только три страны в этом регионе (Бахрейн, Ливия и Йемен) в наименьшей степени подвержены риску в части, касающейся возможного проникновения, акклиматизации и распространения бактерии. Примечательно, что эта проблема не ограничивается средиземноморским регионом. По симптомам болезни и результатам лабораторных анализов было выявлено, что X. fastidiosa связана с ожогом листьев миндаля и болезнью Пирса в виноградниках нескольких провинций Исламской Республики Иран (Amanifar et al., 2014), это говорит о том, что она начнет распространяться на Ближнем Востоке по территориям соседних стран.
В работе Bosso et al. (2016) прогнозируется, что изменение климата в будущем не приведет к дальнейшему увеличению риска X. fastidiosa в большей части средиземноморского региона, однако при прогнозировании риска также следует учитывать полную взаимосвязь «хозяин – переносчик – бактерия». К счастью, активность переносчиков, вероятно, снизится из-за температуры, превышающей оптимальные параметры, и неблагоприятных условий влажности, что недавно было смоделировано в работе Godefroid et al. (2020).
Борьба с X. fastidiosa будет основываться на выработке эффективных стратегий интегрированной защиты растений, включая совершенствование процесса выявления патогена и насекомых-переносчиков, эффективные методы сельскохозяйственного производства и последнее, но не менее важное – эффективные карантинные обработки для борьбы с распространением этого патогена.
9. Оомицеты, включая Phytophthora infestans и Plasmopara viticola (во всем мире)
Потенциальное распространение оомицетов в направлении полюса по причине изменения климата создаст проблему для растениеводства, главным образом, в северном полушарии (Bebber, Ramotowski and Gurr, 2013). Phytophthora infestans – оомицет, вызывающий фитофтороз картофеля и томата, обладает большой способностью адаптироваться к меняющимся условиям, что представляет собой важный фактор, определяющий риск тяжелой эпидемии в будущем. И действительно, по результатам нескольких исследований предполагается увеличение риска появления P. infestans в нескольких странах (Hannukkala et al., 2007; Perez et al., 2010; Skelsey et al., 2016; Sparks et al., 2014), что требует выработки новых стратегий борьбы с этой болезнью и сокращения ее воздействия на продовольственную безопасность, например, более позднее начало сезона выращивания картофеля (Skelsey et al., 2016; Wu et al., 2020).
Исследования в Египте, посвященные влиянию изменения климата на фитофтороз томата и картофеля, показали, как теплая погода зимой влияет на распространенность этой болезни и на борьбу с ней (Fahim, Hassanein and Mostafa, 2003; Fahim et al., 2011). Отмечается, что начало эпидемии фитофтороза томата на одну или две недели раньше будет означать, что потребуется два или три дополнительных опрыскивания для обеспечения эффективной борьбы с этой болезнью. Поэтому в Египте потребуется до трех дополнительных опрыскиваний фунгицидами в течение каждого вегетационного сезона в предстоящие десятилетия (2025–2100 гг.). Что касается фитофтороза картофеля, вызываемого тем же патогеном, сравнение погодных условий и распространенности болезни во время вегетационных сезонов с эпидемией и без эпидемии показало, что влажные и теплые зимы способствуют развитию эпидемии фитофтороза картофеля в Египте. Благоприятные условия зимой способствуют накоплению инокулята патогена на ранних культиварах в начале вегетационного сезона, что приводит к тенденции проявления фитофтороза на более поздних посадках картофеля. Поэтому можно ожидать, что изменение климата будет способствовать эпидемии фитофтороза в будущем. Тем не менее, существует острая необходимость в проведении дальнейших оценок влияния изменения климата на болезни сельскохозяйственных культур в Египте и в других странах Ближнего Востока (Fahim et al., 2011).
Ложная мучнистая роса винограда, которую вызывает оомицет Plasmopara viticola, – еще одна серьезная болезнь, приводящая к значительным производственным потерям от 5 до 30-40 процентов урожая в большинстве регионов выращивания винограда. В случае производства вина ложная мучнистая роса также влияет на его качество. Поскольку во многих из этих регионов умеренный климат с недостаточно оптимальными для патогена температурами, увеличение температуры воздуха окажет благоприятное воздействие на распространение болезни. Поэтому исследования, в которых рассматриваются будущие сценарии изменения климата, прогнозируют возникновение ранних очагов болезни, для борьбы с которыми потребуется больше обработок (Angelotti et al., 2017; Salinari et al., 2006, 2007). Краткосрочные исследования в фитотронах также подтвердили усиление степени воздействия ложной мучнистой росы винограда в смоделированных условиях изменения климата (Pugliese, Gullino and Garibaldi, 2010).
10. Грибы, вырабатывающие микотоксины (во всем мире)
В целом, ожидается, что изменение климата приведет к увеличению присутствия микотоксинов в сельскохозяйственных культурах, однако ввиду разнообразия грибной флоры, связанной с каждой отдельной культурой, и ее взаимодействий с окружающей средой сложно делать выводы без проведения конкретных исследований. Тем не менее, существует множество результатов. Например, в работе Battilani et al. (2016) отмечается, что в Европе глобальное потепление может расширить северные границы риска присутствия афлатоксина в кукурузе, а в работе Van der Fels-Klerx, Liu and Battilani (2016) была проведена количественная оценка влияния климата на появление микотоксинов. В работе Medina et al. (2017) рассматривается влияние изменения климата на микотоксичные грибы посредством изучения влияния трехстороннего взаимодействия между увеличением концентрации CO2 (350–400 по сравнению с 650–1200 частей на миллион), повышением температуры (+2–5 °C) и вызванного засухой стресса на рост и выработку микотоксинов основными грибами, ухудшающими качество зерновых культур и орехов, включая виды Alternaria, Aspergillus, Fusarium и Penicillium. На рост Aspergillus flavus, вырабатывающего афлатоксин B1, по всей видимости, моделируемые условия изменения климата не оказывают влияния. Вместе с тем, в кукурузе была интенсифицирована выработка афлатоксина B1 как in vitro, так и in vivo. С другой стороны, поведение другого вида Aspergillus, приводящего к контаминации целого ряда товаров охратоксином A, а также Fusarium verticillioides, продуцирующего фуминозины, дает основание предполагать, что некоторые виды – более устойчивы к изменению климата, особенно в части выработки микотоксинов.
Изменение климата, наряду с воздействием на широко распространенные грибы, также может повлиять на выработку микотоксинов новыми патогенами, как экспериментально доказано в работе Siciliano et al. (2017a, 2017b) в отношении увеличения количества микотоксинов, продуцируемых видами Alternaria и Myrothecium. Более того, приспособление микотоксичных патогенных грибов к факторам изменения климата может привести к увеличению распространения болезни и, вероятно, к контаминации микотоксинами основных зерновых и других культур. Таким образом, управление рисками, связанными с микотоксинами, в будущем по-прежнему будет большой проблемой (Juroszek and von Tiedemann, 2013b), поскольку изменение климата может ухудшить ситуацию (Miedaner and Juroszek, 2021b).
Нематоды
11. Нематода, повреждающая цитрусовые культуры (Pratylenchus coffeae) (по всему миру)
Нематода Pratylenchus coffeae широко распространена в цитрусовых насаждениях по всему миру. В основном, она заражает растение через питающие корни, по которым подвижные стадии нематоды проникают в кортикальную ткань. Сосудистая ткань остается неповрежденной до тех пор, пока другие организмы не заразят ее в качестве вторичной инфекции (Duncan, 2009). Известно, что нематода уменьшает вес корней цитрусовых наполовину, и при экспериментальном заражении молодых деревьев было установлено замедление роста на 49 – 80 процентов, при этом количество плодов сокращается в диапазоне от трех до двадцати раз (O’Bannon and Tomerlin, 1973). Результаты недавних исследований, посвященных текущему изменению климата в Египте, показывают, что более высокие температуры могут усугубить вред, наносимый этой нематодой корневой системе цитрусовых растений, поскольку скорость ее размножения выше всего при относительно высокой температуре почвы (26–30 °C) (Abd-Elgawad, 2020). При такой температуре завершение жизненного цикла нематоды занимает меньше месяца, и плотность ее популяции может достичь 10 тыс. нематод на грамм корня; эта нематода также может выживать в корнях в почве в течение не менее четырех месяцев. К сожалению, в продаже пока нет саженцев, устойчивых к этой нематоде (Abd-Elgawad, 2020).
12. Соевая цистообразующая нематода (Heterodera glycines) (по всему миру)
Соевая цистообразующая нематода (Heterodera glycines) – возбудитель болезни сои (Glycine max), наносящий самый большой экономический ущерб в Соединенных Штатах Америки и Канаде (Tylka and Marett, 2014). Она также вызывает значительные потери урожая во многих других странах – крупных производителях сои, таких как Аргентина, Бразилия и Китай. Таким образом, она способна вызвать серьезные потери урожая по всему миру.
Глобальное потепление, по всей видимости, будет способствовать расширению ареала нематоды на север (в северном полушарии) и на юг (в южном полушарии), а также увеличению количества поколений в течение сезона выращивания сои (St-Marseille et al., 2019) до тех пор, пока не будут превышены оптимальные для нематоды температурные условия.
Самые важные стратегии борьбы с этим вредным организмом заключаются в использовании устойчивых культиваров (Shaibu et al., 2020) и севооборота (Niblack, 2005). По данным Niblack (2005), севооборот включает не менее трех разных аспектов: в идеале, выращивание сои только один раз в пять лет на одном поле (хотя преимущество севооборота может уменьшиться, если присутствуют сорные растения, которые могут выступать в роли альтернативных хозяев нематоды); использование в широком севообороте сельскохозяйственных культур, в том числе покровных и промежуточных культур, не являющихся растениями-хозяевами; и посадка различных устойчивых или толерантных культиваров сои в разные годы на одном и том же поле с целью сведения к минимуму адаптационного потенциала популяций нематоды.
13. Сосновая стволовая нематода (Bursaphelenchus xylophilus) (Северная Америка и Восточная Азия)
По данным, приведенным в работе Jones et al. (2013), сосновая стволовая нематода B. xylophilus родом из Северной Америки, где она заражает сосны (виды Pinus), но не наносит им серьезного ущерба. Однако в неродной среде, включая Азию (Китай, Республика Корея, Япония и др.) и Европу (несколько случаев обнаружения в Португалии и Испании), это опасный вредный организм, убивающий миллионы сосен. Переносчик этой нематоды – взрослые особи жуков рода Monochamus, которые обитают в хвойных лесах и перелетают на большие расстояния. Ожидается, что глобальное потепление будет все больше благоприятствовать болезни увядания хвойных пород, поскольку жуки рода Monochamus, как и многие другие лесные насекомые (Seidl et al., 2017), выиграют от роста температур, особенно в регионах с умеренным климатом (Ikegami and Jenkins, 2018). Целый ряд проведенных оценок риска показывает, что с увеличением температур участится гибель хвойных деревьев в регионах с умеренным климатом. В средиземноморском регионе, больше всего в Европе подверженном риску, масштабная гибель хвойных деревьев будет иметь серьезные последствия для окружающей среды.
Сорные растения
14. Буддлея Давида (Buddleja davidii) (по всему миру)
Прогнозируется, что ареал инвазивного сорного растения Buddleja davidii в Европе, Северной Америке и Новой Зеландии расширится к концу двадцать первого века из-за ослабления ограничивающих рост факторов, связанных с холодовым стрессом (Kriticos et al., 2011). И наоборот, ареал этого сорняка в Африке, Азии, Южной Америке и Австралии, по прогнозам, уменьшится ввиду увеличения теплового стресса. В целом, прогнозируется сокращение общей площади земли с подходящими условиями произрастания этого сорняка, в среднем, на 11 процентов (8, 10 или 16 процентов в зависимости от используемого сценария изменения климата). К возможным стратегиям адаптации относится определение зон, в которых угроза инвазии возрастет и сократится, для того, чтобы можно было надлежащим образом распределить ресурсы на борьбу с целью ограничения дальнейшего распространения этого сорного растения (Kriticos et al., 2011).
15. Nassella trichotoma (по всему миру)
В текущих климатических условиях сорная трава Nassella trichotoma имеет значительный потенциал к распространению. В будущем сохранятся возможности заселения новых территорий, которые являются подходящими, однако прогнозируется, что к концу двадцать первого века общая площадь подходящей земли во всем мире сократится на 20 – 27 процентов (в зависимости от используемого сценария изменения климата), в основном, в результате прогнозируемого увеличения теплового стресса (Watt et al., 2011). К возможным стратегиям борьбы относятся: определение зон с высоким риском инвазии, применение мер по ограничению распространения семян человеком, а также применение мер борьбы с сорняком для ограничения распространения семян с ветром (Watt et al., 2011).


